
| A. | 用焰色反应鉴別Na2CO3溶液和K2CO3溶液 | |
| B. | 用分液漏斗分离食醋中的乙酸与水 | |
| C. | 用丁达尔现象检验NaCl溶液中是否含有淀粉胶体 | |
| D. | 用NaOH溶液除去Cl2中混有的少量HCl |
分析 A.Na、K的焰色反应分别为黄色、紫色;
B.乙酸与水互溶;
C.丁达尔现象为胶体特有的性质;
D.氯气、HCl均与NaOH溶液反应.
解答 解:A.Na、K的焰色反应分别为黄色、紫色,则焰色反应可鉴别Na2CO3溶液和K2CO3溶液,故A正确;
B.乙酸与水互溶,则不能利用分液漏斗分离,应选蒸馏法,故B错误;
C.丁达尔现象为胶体特有的性质,淀粉溶液为胶体分散系,则用丁达尔现象检验NaCl溶液中是否含有淀粉胶体,故C正确;
D.氯气、HCl均与NaOH溶液反应,不能除杂,应选饱和食盐水、洗气,故D错误;
故选AC.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、物质鉴别及混合物分离提纯等为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:选择题
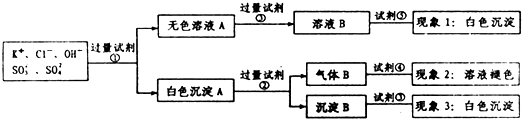
| A. | 试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl | |
| B. | 现象3中白色沉淀是BaSO4 | |
| C. | 试剂②是盐酸,试剂③是硝酸 | |
| D. | 产生现象2的离子方程式是:Br2+2H2O+SO2═4H++2Br-+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
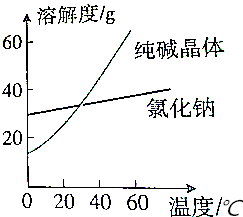
| A. | 蒸馏法 | B. | 苹取法 | C. | 结晶法 | D. | 分液法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
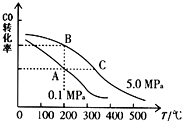 甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的电了式: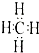 | B. | 乙炔的结构简式:CHCH | ||
| C. | 硫离子的结构示意图: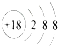 | D. | 中子数为10的原子:${\;}_{8}^{10}$O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
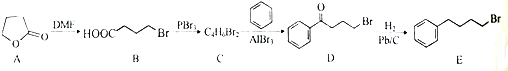
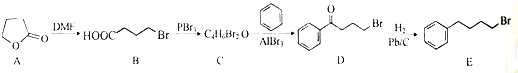
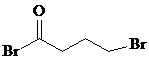 ;由C→D的反应类型是取代反应.
;由C→D的反应类型是取代反应.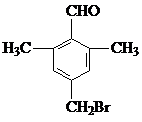 等.
等.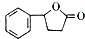 的合成路线流程图(无机试剂任用).合成路线流程图示例如下
的合成路线流程图(无机试剂任用).合成路线流程图示例如下查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 .(不考虑空间构型)
.(不考虑空间构型)查看答案和解析>>
科目:高中化学 来源: 题型:推断题
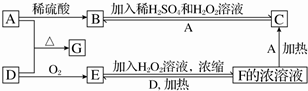
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
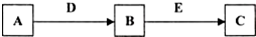
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com