
(本题共10分)水煤气转化反应CO(g)+H2O(g)  CO2(g)+H2 (g)在一定温度下达到化学平衡。完成下列填空:
CO2(g)+H2 (g)在一定温度下达到化学平衡。完成下列填空:
29.写出该反应的平衡常数表达式K=________________。
30.一定温度下,在一个容积不变的密闭容器中发生上述反应,下列说法中能判断该反应达到化学平衡状态的是 (选填编号)。
A.容器中的压强不变
B.1 mol H―H键断裂的同时断裂2 molH―O键
C.v正(CO) = v逆(H2O)
D.c(CO) = c(H2)
31.将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下实验1和实验2的数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 3 |
2 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
3 | 950 | 1 | 2 | — | — | — |
(1)由实验组1的数据可知,平衡时CO的转化率为 %。
(2)由实验组1和2的数据可分析,压强对该可逆反应的影响是 。
(3)有了实验组1和2的数据,再设计实验3,其目的是 。
29.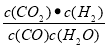 (2分); 30. B、C (2分);31.(1)40%(2分)。
(2分); 30. B、C (2分);31.(1)40%(2分)。
(2)增大压强加快反应速率;增大压强化学平衡不移动(或反应物的转化率不变。合理即可)(2分)。
(3)温度对化学反应速率的影响;该反应是吸热还是放热反应(温度对化学平衡移动的影响)(2分)
【解析】
试题分析:29.反应CO(g)+H2O(g)  CO2(g)+H2 (g)的平衡常数的表达式是K=
CO2(g)+H2 (g)的平衡常数的表达式是K=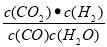
30.A.由于该反应是反应前后气体体积相等的反应,所以在任何时刻都存在容器中的压强不变。故容器内的气体压强不变,不能作为判断平衡的标志,错误;B.1 mol H―H键断裂,就会产生2mol的H —O键,还同时断裂2 molH―O键,说明水的浓度不变,作为反应达到平衡状态,正确;C.在任何时刻都存在v正(CO) = v正(H2O),同时还存在v正(CO) = v逆(H2O),说明v正(H2O) = v逆(H2O),反应处于平衡状态,正确;D.c(CO) = c(H2)时,反应可能处于平衡状态,也可能不处于平衡状态,这与加入的物质的多少有关,错误;故选项是B、C。
31.(1)由实验组1的数据可知,平衡时CO的转化率为[(4—2.4)÷4]×100%=40%;(2)根据实验2可知CO的平衡转化率是:[(2—1.2)÷2]×100%=40%;物质的平衡含量不变,但是达到平衡所需要的时间较长,反应速率减慢。说明增大压强加快反应速率;增大压强化学平衡不移动,物质的转化率不发生改变;(3)有了实验组1和2的数据,再设计实验3,其目的是在物质浓度不变时,改变温度,判断温度对化学反应速率的影响;温度对化学平衡移动的影响;该反应是吸热还是放热反应的判断的知识。
考点:考查化学平衡常数的的表达、平衡状态的判断、物质的平衡转化率的计算及温度、压强对化学反应速率、化学平衡移动的影响的知识。


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:填空题
(14分)铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
(1)铝在反应中容易失去电子,发生 反应(填氧化或还原),生成铝离子,铝离子的结构示意图是 。
(2)生产中曾用铝热反应焊接钢轨,写出铝与氧化铁发生反应的化学方程式为并标出电子转移的方向和数目: 。
(3)胃舒平是治疗胃酸过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示): ;
(4)在同温同压下,等质量的铝分别投入足量的稀盐酸和NaOH溶液中,产生气体的体积之比为 。
(5)铝合金在空气中很稳定,可以制造多种建筑型材。向一只小烧杯里加入少量CuSO4溶液,把一小块铝合金浸入溶液中,1~2分钟后将铝合金取出,无明显现象。将另一小块铝合金先放入NaOH溶液里,片刻后取出,用蒸馏水冲洗后浸入CuSO4溶液里,1~2分钟后将铝片取出,发现铝片表面有亮红色的固体附着,NaOH溶液的作用是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省等四校高一上学期期中联考化学试卷(解析版) 题型:填空题
(6分)在下列物质中选择溶于水后可以电离的物质,并写出相应的电离方程式(有几个写几个):①硝酸铵(NH4NO3) ②葡萄糖[C6H12O6] ③氢氧化钡[Ba(OH)2] ④硫酸(H2SO4) ⑤四氯化碳(CCl4)
。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省等四校高一上学期期中联考化学试卷(解析版) 题型:选择题
N2O是一种有甜味、能溶于水、能助燃的无色气体,它能刺激神经使人发笑,俗称“笑气”;它具有麻醉作用,曾用作牙科麻醉剂。现有等物质的量的笑气和二氧化碳,下列数值不一定相同的是
A.分子数 B.电子数 C.原子数 D.中子数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海理工大学附中高三上学期月考化学试卷(解析版) 题型:计算题
(本题共14分)已知:硝酸铜受热易分解。
170℃时,2Cu (NO3)2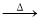 2CuO
2CuO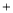 4NO2↑
4NO2↑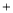 O2↑开始分解,至250℃分解完全。(其中2NO2
O2↑开始分解,至250℃分解完全。(其中2NO2 N2O4,2NO2
N2O4,2NO2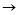 2NO
2NO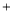 O2等反应忽略不计)。
O2等反应忽略不计)。
800℃时,4CuO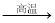 2Cu2O
2Cu2O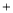 O2↑ 开始分解,至1000℃以上分解完全。
O2↑ 开始分解,至1000℃以上分解完全。
54.取5.64g无水硝酸铜,加热至1000℃以上,将生成的气体导入足量的NaOH溶液充分吸收后,还有逸出的气体是 (填分子式),体积(标准状况)为 ;将吸收液加水稀释到100mL,此溶液中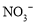 的物质的量浓度为 。
的物质的量浓度为 。
55.取5.64g无水硝酸铜加热至某温度分解后的残留固体中含有1.60g CuO,则残留固体的质量可能是 。
实验证明,当温度达到1800℃时,Cu2O也会发生分解:2Cu2O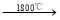 4Cu
4Cu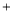 O2↑
O2↑
56.取8.00g CuO,加热到1800℃左右,冷却后称得质量为6.88g,通过计算求出反应后剩余固体中各成分的物质的量之比。
57.取8.00g CuO,通入一定量H2并加热,使其部分还原为Cu和Cu2O,且其中n (Cu2O)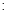 n (Cu)
n (Cu)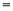 x。将此混合物溶于足量的稀硫酸中(Cu2O
x。将此混合物溶于足量的稀硫酸中(Cu2O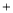 2H
2H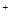
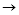 Cu
Cu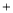 Cu
Cu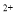
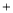 H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海理工大学附中高三上学期月考化学试卷(解析版) 题型:选择题
已知:①向KMnO4晶体中滴加盐酸,产生黄绿色的气体;②向FeCl2溶液中通入少量的实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
A.上述实验证明氧化性:MnO4— > Cl2 > Fe3+ > I2
B.上述实验中发生的反应都是氧化—还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②可以证明Fe2+既有氧化性又有还原性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海理工大学附中高三上学期月考化学试卷(解析版) 题型:选择题
物质制备过程中离不开物质的提纯。以下除杂方法不正确的是
选项 | 目的 | 实验方法 |
A | 除去Na2CO3固体中的NaHCO3 | 置于坩埚中加热至恒重 |
B | 除去NaCl中少量KNO3 | 将混合物制成热饱和溶液,冷却结晶,过滤 |
C | 除去CO2中的HCl气体 | 通过NaHCO3(aq,饱和),然后干燥 |
D | 除去C2H5Br中的Br2 | 加入足量Na2SO3(aq),充分振荡,分液 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三12月月考理综化学试卷(解析版) 题型:选择题
下图中甲池是以甲醇为原料,KOH为电解质的高效燃料电池,电化学过程的如图。

下列说法中不正确的是
A.甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O
B.若乙池中为足量AgNO3溶液,则阳极的电极反应为: 4OH--4e- = 2H2O+O2↑
C.若乙池中为一定量CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移的电子数为0.2NA
D.常温常压下,1 g CH3OH燃料生成CO2和液态H2O时放热22.68 kJ,表示该反应的热化学方程式为:CH3OH(l)+1.5O2(g)==CO2(g)+2H2O(l) ΔH= -725.80 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴市高二10月月考化学试卷(解析版) 题型:选择题
设反应C+CO2  2CO(正反应吸热)反应速率为v1,N2+3H2
2CO(正反应吸热)反应速率为v1,N2+3H2  2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为
A.同时增大 B.同时减小
C.v1增大,v2减小 D.v1减小,v2增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com