
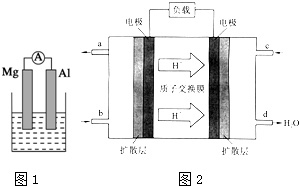
 据图回答下列问题:
据图回答下列问题:分析 I、(1)镁比铝活泼,若烧杯中溶液为稀硫酸,镁为负极,铝为正极;
(2)铝和与氢氧化钠溶液反应,若烧杯中溶液为氢氧化钠溶液,铝为负极,镁为正极;
Ⅱ、Al遇浓硝酸发生钝化,Cu与浓硝酸发生氧化还原反应,则Cu失电子作负极,Al作正极,据此分析;
Ⅲ、①根据氢离子移动方向知,右侧电极为正极,左侧电极为负极,负极上通入燃料;
②负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应.
解答 解:I、(1)镁比铝活泼,若烧杯中溶液为稀硫酸,形成原电池反应,镁为负极,铝为正极,负极发生Mg-2e-=Mg2+,可观察到Mg逐渐溶解,Al片上有气泡冒出,指针偏,
故答案为:Mg逐渐溶解,Al片上有气泡冒出,指针偏转;Mg-2e-=Mg2+;
(2)铝和与氢氧化钠溶液反应,若烧杯中溶液为氢氧化钠溶液,铝为负极,镁为正极,负极生成NaAlO2,正极生成氢气,反应的总方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:Al;2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
Ⅱ、Al遇浓硝酸发生钝化,Cu与浓硝酸发生氧化还原反应,则Cu失电子作负极,Al作正极,正极上硝酸根离子得电子生成二氧化氮,则正极上的电极反应为NO3-+e-+2H+=NO2↑+H2O;
故答案为:NO3-+e-+2H+=NO2↑+H2O;
Ⅲ、①据氢离子移动方向知,右侧电极为正极,c口通氧气,左侧电极为负极,b口为负极上通入燃料甲醇,故答案为:CH3OH;O2;
②正极上氧气得电子和氢离子反应生成水,电极反应式为:O2+4H++4e-=2H2O,负极上甲醇失电子和水反应生成二氧化碳和氢离子,电极反应式为2CH3OH-12e-+2H2O=2CO2↑+12H+,故答案为:O2+4H++4e-=2H2O.
点评 本题综合考查原电池知识,为高频考点,侧重于学生的分析能力的考查,注意把握铝与氢氧化钠反应的特点,为解答该题的关键,注意相关基础知识的积累,侧重于正负极的判断和电极方程式的书写,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 丙烯分子中3个碳原子都是sp3杂化 | |
| B. | 丙烯分子存在非极性键 | |
| C. | 丙烯分子有6个σ键,1个π键 | |
| D. | 丙烯分子中3个碳原子在同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热--检验混合物中是否含有甲醛 | |
| B. | 向CH3CH2Br中滴入AgNO3溶液以检验溴元素 | |
| C. | 苯不能与溴水发生取代反应,用苯能萃取溴的四氯化碳溶液中的溴 | |
| D. | 利用核磁共振氢谱,可以鉴别CH3OCH3和CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X位于元素周期表中第2周期ⅤA族 | |
| B. | X元素有-3、+5两种化合价 | |
| C. | X元素在元素周期表中的族序数肯定为奇数 | |
| D. | X元素最高价氧化物对应的水化物可以表示为H3XO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧反应都是放热反应 | |
| B. | 对于可逆反应:aA(g)+bB(g)?bC(g)+dD(g),如果正反应放热,逆反应一定吸热 | |
| C. | 氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量 | |
| D. | 只有放热的氧化还原反应才可以设计为原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH3OH+3O2→2CO2+4H2O | B. | NaOH+HCl=NaCl+H2O | ||
| C. | Zn+2HCl=ZnCl2+H2↑ | D. | 4Al+3O2+6H2O=4Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ①④⑥ | C. | ②④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y形成化合物时X显负价,Y显正价 | |
| B. | 第一电离能X大于Y | |
| C. | 最高价氧化物对应的水化物的酸性:X强于Y | |
| D. | 气态氢化物的稳定性:HmX强于HmY |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
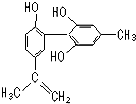 坚决反对运动员服用兴奋剂是保证运动会公平公正的重要举措之一.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
坚决反对运动员服用兴奋剂是保证运动会公平公正的重要举措之一.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 该分子中的所有碳原子不可能共平面 | |
| C. | 滴入KMnO4(H+)溶液,观察紫色变浅,是因为结构中存在碳碳双键 | |
| D. | 1 mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别为4 mol、7 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com