
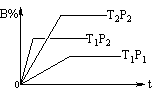 已知某可逆反应:mA(g) + nB(g)
已知某可逆反应:mA(g) + nB(g) pC(g),在密闭容器中进行,下图表示在不同时间t、温度T、压强p与反应物B的百分含量的关系曲线,下列判断正确的是
pC(g),在密闭容器中进行,下图表示在不同时间t、温度T、压强p与反应物B的百分含量的关系曲线,下列判断正确的是
A.T2>T1 P1>P2 m+n>P △H <0
B.T1>T2 P1<P2 m+n<P △H >0
C.T1<T2 P1<P2 m+n<P △H <0
D.T1>T2 P1<P2 m+n>P △H >0
科目:高中化学 来源: 题型:
下列化合物分子中,在核磁共振氢谱图中能给出二种信号的是( )
A.CH3CH2CH3 B.CH3COCH2CH3 C.CH3CH2OH D.CH3OCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
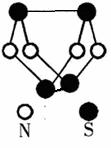
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是( )
A.该物质与S2N 2互为同素异形体
B.该物质的分子中既有极性键又有非极性键
C.该物质可能是离子化合物
D.该物质的一个分子中含有9个N—S键
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应M + N = P,如果温度每升高10℃,化学反应速率增加到3倍,在20℃时完成该反应的30%需要81 min,若将温度升高到40℃,完成该反应的30%需要时间为( )
A.9 min B.27 min C.13.5 min D.3 min
查看答案和解析>>
科目:高中化学 来源: 题型:
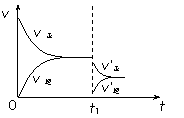
在密闭容器中发生反应2SO2(g) + O2(g) 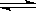 2SO3(g) △H<0。右图是该反应化学反应速率随时间变化的图象,推断在t1时刻突然变化的条件可能是( )
2SO3(g) △H<0。右图是该反应化学反应速率随时间变化的图象,推断在t1时刻突然变化的条件可能是( )
A.催化剂失效 B.增大容器的体积
C.降低体系温度 D.减小生成物的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)对于下列反应:2SO2(g) + O2(g) 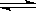 2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
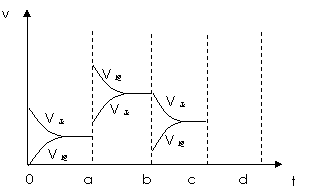
(2)下图表示在密闭容器中反应:2SO2+O2 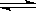 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处。
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处。
 |
(3)以上反应达平衡后,
若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应正向为 反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均相对分子质量
比原平衡时 (填“增大”、“减小”或“相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=-Q1 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l) △H=-Q2 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g) △H=-Q3 kJ/mol
判断Q1、Q2、Q3三者关系正确的是
A. Q1>Q2>Q3 B. Q1>Q3>Q2 C. Q3>Q2>Q1 D. Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2L的密闭容器中加入4mol A和6mol B,发生如下反应:2A(g)+3B(g) 4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L。下列说法正确的是( )
4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L。下列说法正确的是( )
A、前10min反应的平均速率V(C)=0.10mol/L·min
B、反应达平衡时B的平衡浓度是1.5mol/L
C、恒温下将反应容器体积缩小一半,则D的平衡浓度小于1.0mol/L
D 、10min后向容器中加入A,重新平衡时A的转化率一定大于50%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列观点不正确的是 ( )
A.化学是一门以实验为基础的科学
B.从宏观看,物质有时处在相对静止状态,但从微观看,则是永恒运动的
C.运用分类的方法,可根据物质所属的类别预测物质的性质
D.世界是由物质构成的,物质都是由分子和原子构成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com