
| A. | 能用适当的酸碱指示剂来判断 | |
| B. | 参加反应的酸中的H+离子总量和碱中OH-离子总量相等 | |
| C. | 反应混合液的pH=7 | |
| D. | 反应的热效应即为中和热 |
分析 A.无法用指示剂判断酸碱恰好反应,指示剂只能粗略判断滴定终点.
B.酸碱恰好反应时,酸中氢离子与碱溶液中的氢氧根离子的物质的量一定相等;
C.酸碱恰好反应时,溶液的pH不一定为7,如氢氧化钠与醋酸反应生成醋酸钠,醋酸钠溶液呈碱性.
D.在稀溶液中,酸跟碱发生中和反应则生成1molH2O,这时的反应热叫做中和热.
解答 解:A.指示剂只能粗略判断滴定终点,无法用指示剂判断酸碱溶液恰好反应,故A错误;
B.在室温下进行中和滴定,酸和碱恰好完全反应时,参加反应的酸中的H+离子总量和碱中OH-离子总量相等,故B正确;
C.室温下酸和碱恰好完全反应时,溶液的pH不一定等于7,如醋酸与NaOH溶液的反应,恰好反应时生成醋酸钠,醋酸根离子部分水解,溶液呈碱性,故C错误;
D.在稀溶液中,酸跟碱发生中和反应则生成1molH2O,这时的反应热叫做中和热,所以酸和碱恰好完全反应时,反应的热效应不一定为中和热,故D错误;
故选B.
点评 本题考查了中和滴定的操作方法,题目难度不大,明确酸碱恰好中和反应的含义为解答关键,注意熟练掌握中和滴定操作方法,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| 选项 | ① | ② | ③ | Ⅱ中的现象 | 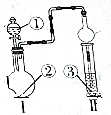 |
| A | 浓盐酸 | 碳酸钙 | 滴有酚酞的稀碳酸钠溶液 | 溶液由红色最终变为浅红色 | |
| B | 浓氨水 | 氧化钙 | 氯化铝溶液 | 先产生白色沉淀,后沉淀溶解 | |
| C | 冰醋酸 | 乙醇和浓硫酸 | 饱和碳酸钠溶液 | 溶液分层,上层为油状液体 | |
| D | 浓硝酸 | 铜 | 硅酸钠溶液 | 有胶状物生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量碳酸钠晶体(Na2CO3•10H2O)的时间太长,而且暴露在空气中 | |
| B. | 向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤 | |
| C. | 定容时仰视刻度线 | |
| D. | 溶解后未冷却到室温,立即转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验次数编号 | 盐酸溶液体积V(mL) | 氢氧化钠溶液体积 V(mL) |
| 1 | 22.4 | 10.00 |
| 2 | 22.60 | 10.00 |
| 3 | 26.00 | 10.00 |
| 4 | 22.50 | 10.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
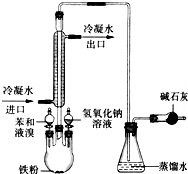 如图是实验室制取溴苯的装置图.
如图是实验室制取溴苯的装置图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol•L-1醋酸溶液与 0.1 mol•L-1醋酸溶液中c(H+)之比 | |
| B. | (NH4)2SO4溶液中c(NH4+)和c(SO42-)的物质的量浓度之比 | |
| C. | pH=2的盐酸和pH=12的Ba(OH)2溶液中溶质的物质的量浓度之比 | |
| D. | 0.2 mol/LCH3COONa溶液与 0.1 mol•L-1Na2CO3溶液中c(CH3COO-)与c(CO32-)之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
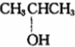 ⑨${\;}_{6}^{13}$C
⑨${\;}_{6}^{13}$C 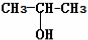 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com