
| A、它能够导电 |
| B、它的pH=0 |
| C、它含有人体所需的矿物质和多种微量元素 |
| D、它清洁、纯净,但长期饮用对人健康无益 |
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
| 物质 | X | Y | Z |
| 初始浓度/mol?L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、反应达到平衡时,X的转化率为50% |
| B、改变温度可以改变此反应的平衡常数 |
| C、反应可表示为X+3Y?2Z,平衡常数为1600 |
| D、增大压强使平衡向生成Z的方向移动,平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④⑥⑦ | B、②③⑤⑧ |
| C、①②⑧ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、③>②>① |
| B、①>②>③ |
| C、②>③>① |
| D、①=②=③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯、苯、氯乙烯所有原子都在同一个平面上 |
| B、乙醇、乙酸均能与Na反应放出H2,二者分子中有相同的官能团 |
| C、葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体 |
D、苹果醋是一种常见的有机酸,其结构简式为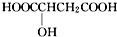 在标准状况下,1mol苹果醋与足量的金属钠反应生成的11.2L氢气 在标准状况下,1mol苹果醋与足量的金属钠反应生成的11.2L氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.3mol |
| B、常温常压下,22.4LO2所含的原子数小于2NA |
| C、标准状况下,11.2LCH3CH2OH中含有0.5NA个分子 |
| D、1.8g的NH4+离子中含有的电子数NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH的电离度减少,PH减小 |
| B、平衡向生成CH3COOH移动,c(H+)减小 |
| C、CH3COOH电离度增大,c(H+)增大 |
| D、电离平衡向生成CH3COO-、H+方向移动,PH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④ | B、②③⑥ |
| C、①②④⑤ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com