
 H2+CO,其中,水是 剂.硫在氧气中燃烧的化学方程式是 ,其中,硫是 剂.
H2+CO,其中,水是 剂.硫在氧气中燃烧的化学方程式是 ,其中,硫是 剂.  提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
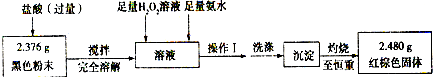
 在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.现用下图中甲、乙两套仪器装置制取上述铁的氧化物和细铁粉.制取上述铁的氧化物和细铁粉时必须使用普通铁粉和6mol?L-1盐酸,其他试剂任选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热装置等以及仪器中所装的试剂在图中均已略去).
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.现用下图中甲、乙两套仪器装置制取上述铁的氧化物和细铁粉.制取上述铁的氧化物和细铁粉时必须使用普通铁粉和6mol?L-1盐酸,其他试剂任选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热装置等以及仪器中所装的试剂在图中均已略去).
| ||
| ||

查看答案和解析>>
科目:高中化学 来源:甘肃省天水市一中2009-2010学年高二上学期期末考试化学试卷(理) 题型:038
镁、铝都是较活泼的金属,在一定条件下能与氧、氮等起反应.镁铝合金粉可用作烟火材料.
(a)取此合金粉与足量的稀硫酸反应,在大气压为101325 Pa,温度为25℃时,在水面上收集到气体的体积为0.5052 L.
(b)另取等量的此合金粉在氧气中燃烧,将燃烧产物用足量的稀硫酸处理,将不溶物用水洗净烘干,称重为0.3399克.
(c)再取等量的此合金粉使之在空气中燃烧,将燃烧产物用足量的稀氢氧化钠溶液处理,将溶液滤去,残渣先用氢氧化钠溶液洗涤,然后用水洗净,再将残渣在高温下灼烧至恒重,得0.7090克.(25℃时,饱和水蒸气压为3167 Pa,R=8.314 kPa·L·mol-1·K-1).
(1)求产生H2的物质的量;
(2)求在氧气中燃烧时生成MgO的质量;
(3)写出(c)中的各步化学反应方程式;
(4)求在空气中燃烧时生成Al2O3的质量;
(5)求合金粉中Al的百分含量.
查看答案和解析>>
科目:高中化学 来源:期末题 题型:实验题
 3Cu+N2+3H2O
3Cu+N2+3H2O  Cu+Cu2+ 。
Cu+Cu2+ 。 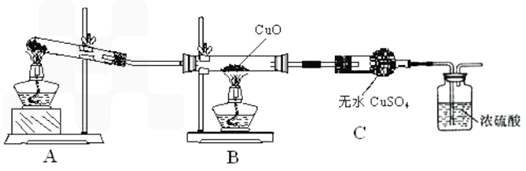
查看答案和解析>>
科目:高中化学 来源: 题型:
下列中学常见实验的现象或表述正确的是 ( )
A.在酒精灯上灼烧用砂纸打磨过的铝箔(已除氧化膜),会发现熔化的铝不断滴落
B.钠与硫酸铜溶液反应时的现象可用浮、熔、游、响、红色固体进行简单描述
C.铁和镁均是较活泼的金属,易被空气中的氧气氧化而形成一层致密的氧化膜
D.铁和高温水蒸气的实验中,可用干净的细铁丝代替还原铁粉进行实验
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com