
【题目】下列实验事实不能用平衡移动原理解释的是( )
A.工业合成氨反应中加压有利于提高氨气的产率
B.将NO2球浸泡在冷水和热水中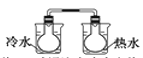
C.红棕色的NO2 ,加压后颜色先变深后变浅
D.
【答案】D
【解析】
勒夏特列原理是:如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡将向着能够减弱这种改变的方向移动。勒夏特列原理适用的对象应存在可逆过程,若与可逆过程无关,则与平衡移动无关,则不能用勒夏特列原理解释。
A. 工业合成氨反应为N2+3H22NH3,加压平衡向气体体积减小的方向移动,则该反应加压会向着正反应方向移动,即生成氨气的方向移动,有利于提高氨气的产率,能用勒夏特利原理解释,A项错误;
B. NO2球中存在平衡2NO2N2O4 ΔH<0,升高温度平衡向吸热反应方向移动,即逆反应方向移动,混合气体颜色变深,降低温度平衡向放热反应方向移动,即正反应方向移动,混合气体颜色变浅,能用勒夏特利原理解释,B项错误;
C. 红棕色的NO2气体中存在平衡2NO2N2O4,加压体积减小,NO2浓度增大,混合气体颜色变深,但压强增大平衡正向移动,NO2浓度又减小,则颜色又变浅,能用勒夏特利原理解释,C项错误;
D. 由H2(g)、I2(g)、HI(g)气体组成的平衡体系中存在可逆反应H2(g)+I2(g)2HI(g),是一个反应前后气体物质的量不变的反应,体积减小加压,H2(g)、I2(g)、HI(g)浓度均增大,但是平衡不会移动,颜色加深仅是由体积减小,I2(g)浓度增大造成的,不能用勒夏特利原理解释,D项正确;
答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氰化物是剧毒物质,传统生产工艺的电镀废水中含一定浓度的CN-,无害化排放时必须对这种废水进行处理。 可采用碱性条件下的Cl2氧化法处理这种废水,涉及两个反应:反应i,CN- +OH-+Cl2![]() OCN- +Cl-+H2O(未配平);
OCN- +Cl-+H2O(未配平);
反应ii,OCN- + OH-+ Cl2![]() X + Y + Cl-+ H2O(未配平)。
X + Y + Cl-+ H2O(未配平)。
其中反应i中N元素的化合价没有变化,常温下,X、Y是两种无毒的气体。下列判断正确的是( )
A.反应i中氧化剂与还原剂的化学计量数之比为1: 1
B.X、Y是CO2、N2,且均为反应ii的氧化产物
C.该废水处理工艺过程中须采取措施,防止Cl2逸出到空气中
D.处理c(CN-) =0.000 1 mol·L-1的废水106 L,消耗标况下的Cl2 4.48×103L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
B. 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
C. 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
D. 对于2HI(g)![]() H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到目的的是( )
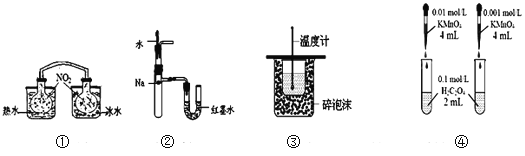
A. 装置①依据两容器内气体颜色变化,不能判断反应2NO2(g)![]() N2O4(g)平衡移动的方向
N2O4(g)平衡移动的方向
B. 装置②依据U管两边液面的高低判断Na和水反应的热效应
C. 装置③测定中和热
D. 装置④依据褪色快慢比较浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组设计了如图甲所示的数字化实验装置,研究常温下,向1L 0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的粒子的 物质的量分数与溶液pH的关系如图乙所示,(已知HA=H++HA- HA- ![]() H++A2-)则下列说法中正确的是( )
H++A2-)则下列说法中正确的是( )

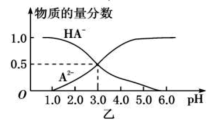
A.pH=3.0时,可以计算出Ka2= 10 -3
B.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L
C.该实验左边的滴定管为碱式滴定管,用来盛装NaOH溶液,烧杯中并加酚酞作指示剂
D.常温下,将等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是

A.该硫酸试剂的物质的量浓度为18.4 mol/L
B.稀释该硫酸时应把水倒入硫酸中,边倒边搅拌
C.50 mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46 mol
D.标准状况下2.7 g Al与足量的该硫酸反应可得到H2 3.36 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以异丁烯为原料合成某二酸的合成路线如图:
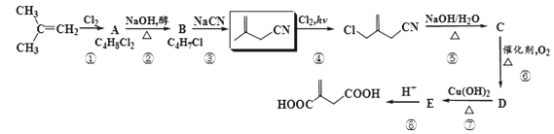
已知:R-CH2CN![]() R-CH2COONa+NH3
R-CH2COONa+NH3
(1)A的系统命名是__,B的官能团名称__。
(2)步骤③的反应类型是__。
(3)同一有机物中的两个同种官能团在反应时,一者参与反应占绝大多数,另一者几乎不反应,这被称之为“位置专一性”。请从反应物结构角度,简要解释步骤②中消去氯原子时的位置专一性:__。
(4)步骤⑤的产物C经酸化后,可发生分子内酯化,写出该内酯的结构简式___。
(5)写出步骤⑥的化学方程式__。
(6)均符合下列条件B的同分异构体为__。
a.所有碳原子一定共平面;b.核磁共振氢谱有3组峰。
(7)利用题目给的信息,写出由异丁烯为原料,两步合成![]() 的路线流程___。
的路线流程___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单斜硫和正交硫是硫的两种同素异形体。下列说法正确的是

A.S(s,单斜)═S(s,正交) ΔH3=-0.33 kJmol1
B.单斜硫比正交硫稳定
C.相同物质的量的正交硫比单斜硫所含有的能量高
D.①式表示断裂 1 mol O2 中的共价键所吸收的能量比形成 1 mol SO2 中的共价键所放出的能量多 297.16 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮气是制备含氮化合物的一种重要物质,而含氮化合物的用途广泛,如图表示两个常见固氮反应的平衡常数对数值(lg K)与温度的关系:①N2+3H2![]() 2NH3,②N2+O2
2NH3,②N2+O2![]() 2NO。
2NO。

根据图中的数据判断下列说法正确的是( )
A.反应①和②均为放热反应
B.升高温度,反应①的反应速率减小
C.在常温下,利用反应①固氮和利用反应②固氮反应程度相差很大
D.在1 000 ℃时,反应①和反应②体系中N2的浓度一定相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com