
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
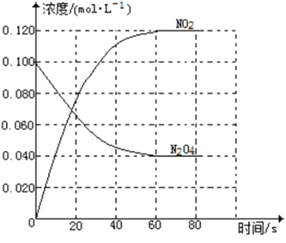
(1)反应的△H______0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为___________molL-1s-1反应的平衡常数K1为___________。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10s又达到平衡。
①T_______100℃(填“大于”“小于”),判断理由是_____。
②列式计算温度T是反应的平衡常数K2___________
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___________(填“正反应”或“逆反应”)方向移动,判断理由是___________。
【答案】大于 0.001 0.36 mol·L—1 大于 反应正方向吸热,反应向吸热方向进行,故温度升高 平衡时,c(NO2)=0.120 mol·L—1+0.002 mol·L—1·s—1×10s×2=0.160mol·L—1
c(N2O4)=0.040 mol·L—1—0.002 mol·L—1·s—1×10s=0.02 mol·L—1
K2=0.160mol·L—1)2/0.020mol·L—1=1.3mol·L—1 逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动
【解析】
(1)根据题意知,随温度升高,混合气体的颜色变深,二氧化氮的浓度增大,说明平衡向正反应方向移动;当其他条件不变时,升高温度,平衡向吸热反应方向移动,说明正反应为吸热反应,故△H大于0。根据题给图像知,0-60s时段,N2O4的物质的量浓度变化为0.060 mol·L-1,根据公式v=△c/△t计算,v (N2O4)= 0.060 mol·L-1/60s=0.001 mol·L-1·s-1;分析题给图像知,二氧化氮的平衡浓度为0.120 mol·L-1,四氧化二氮的平衡浓度为0.040 mol·L-1,K1= [NO2]2/[N2O4]=0.36 mol·L-1;
(2)①根据题意知,改变反应温度为T后,c(N2O4)以0.0020 molL-1s-1的平均速率降低,即平衡向正反应方向移动,又反应正方向吸热,反应向吸热方向进行,故为温度升高,T大于1000C,答案为:大于;反应正方向吸热,反应向吸热方向进行,故温度升高;
②根据题意知,平衡时,c(NO2)=0.120 mol·L-1+0.002 mol·L-1·s-1×10s×2=0.160mol·L-1,c(N2O4)=0.040 mol·L-1-0.002 mol·L-1·s-1×10s=0.02 mol·L-1,K2=(0.160mol·L-1)2/0.020mol·L-1=1.3mol·L-1;
(3)温度为T时,反应达平衡,将反应容器的体积减小一半,即增大压强,当其他条件不变时,增大压强,平衡向气体物质平衡向气体物质系数减小的方向移动,即向逆反应方向移动,答案为:逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知101kPa时的辛烷的燃烧热为5518kJ/mol,强酸与强碱在稀溶液中发生反应时的中和热为57.3kJ/mol,则下列热化学方程式书写正确的是
①C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l);△H=+5518kJ/mol;
O2(g)=8CO2(g)+9H2O(l);△H=+5518kJ/mol;
②C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l);△H=﹣5518kJ/mol;
O2(g)=8CO2(g)+9H2O(l);△H=﹣5518kJ/mol;
③![]() H2SO4(aq)+Ba(OH) 2(aq)=
H2SO4(aq)+Ba(OH) 2(aq)=![]() BaSO4(s)+H2O(l);△H=﹣57.3kJ/mol;
BaSO4(s)+H2O(l);△H=﹣57.3kJ/mol;
④H+(aq)+OH﹣(aq)=H2O(l);△H=﹣57.3kJ/mol.
A.①③B.②③C.②④D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以食盐、氨气、二氧化碳等物质为原料制取纯碱。
(1)实验室提纯粗盐的一个重要环节是除去粗盐水中的杂质阳离子(主要含Ca2+、Mg2+),提纯该粗盐时,可考虑在粗盐水中依次加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。A____ 、B_____。
(2)氨气分子的空间构型为_____,其中N原子采用_____杂化方式,二氧化碳中心原子C采用_____杂化方式。
(3)上述实验涉及的元素中,Ca基态原子电子排布式为__________________。
(4)上述实验涉及的元素中,O2-、Na+、Cl-中半径最小的是__________。
(5)制取纯碱时,向饱和食盐水中通入气体,即可得到小苏打的沉淀物,氨气与二氧化碳通入的先后顺序是:_________,因为:___________
(6)写成工业上以食盐、氨气、二氧化碳等物质为原料制取小苏打反应的化学方程式:______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污染。
(1)下列各项符合“绿色化学”要求的是____。
A.处理废弃物 B.治理污染点 C.减少有毒物 D.杜绝污染源
(2)在我国西部大开发中,某地为筹建一大型化工基地,征集到下列方案,其中你认为可行的是____。
A.建在西部干旱区可以脱贫致富
B.应建在水资源丰富和交通方便且远离城市的郊区
C.企业有权自主选择厂址
D.不宜建在人口稠密的居民区
(3)某化工厂排放的污水中含有Mg2+、Fe3+、Cu2+、Hg2+四种离子。某同学设计了从该污水中回收纯净的金属铜的方案。

在能制得纯铜的方案中,哪一步操作会导致环境污染?___。应增加哪些措施防止污染______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是( )
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是( )
A.容器内压强不再改变B.v(H2O)=v(H2)
C.气体的密度不再改变D.反应不再进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

(1)写出该反应的化学方程式__________。
(2)计算反应开始到10 s,用X表示的反应速率是__________,Y的转化率为______。
(3)下列叙述中能说明上述反应达到平衡状态的是____。
A.当X与Y的反应速率之比为1:1
B.在混合气体中X的质量百分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的的密度不随时间的变化而变化
E.X、Y、Z的浓度之比为1:1:2
(4)当反应达到平衡时,用Y表示的正反应速率v(正)与用Z表示的逆反应速率v(逆)的关系是_____________。
(5)为使该反应的反应速率增大,可采取的措施是______.
a.恒容时充入Ne b.适当升高温度
c.缩小容器的体积 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在工业上可用含SiO2、CeO2和Fe2O3的废料作原料来获得硫酸铁铵晶体(Fe2(SO4)3·2(NH4)2 SO4·3H2O),同时可回收CeO2,工艺流程设计如下
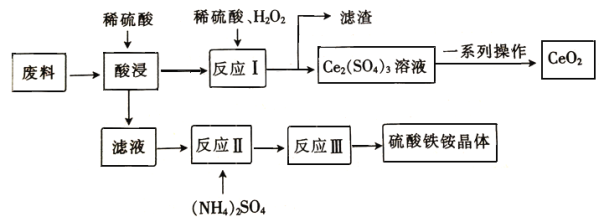
已知: ①SiO2、CeO2不溶于稀硫酸;②酸性条件下,CeO2可与H2O2反应;③“反应Ⅰ”所得溶液中含有Ce3+;④碱性条件下,NH4+与OH-结合生成NH3·H2O。
请回答下列问题
(1)“酸浸”时未发生的反应 物质是__________________(填化学式)。
(2)“滤液”中含有的阳离子有___________________(填离子符号)。
(3)写出“反应Ⅰ”的化学方程式:________________________________________。
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是__________________(填化学式)。
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型污水处理装置模拟细胞内生物电的产生过程,可将酸性有机废水的化学能直接转化为电能。下列说法中不正确的是

A. M极作负极,发生氧化反应
B. 电子流向:M→负载→N→电解质溶液→M
C. N极的电极反应:O2+4H++4e-=2H2O
D. 当N极消耗5.6L(标况下)气体时,最多有NA个H+通过阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖。
(1)基态Fe2+的核外电子排布式为_________________。
(2)氟、氧、砷三种元素中电负性值由大到小的顺序是__________(用相应的元素符号填空)。
(3)Fe(SCN)3溶液中加人NH4F,发生如下反应:Fe(SCN)3+6NH4F=(NH4)3FeF6+3NH4SCN。
①(NH4)3FeF6存在的微粒间作用力除共价键外还有_________(选填序号,下同)。
a.配位键 b.氢键 c.金属键 d.离子键
②已知SCN一中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为_____________,该原子团中![]() 键与
键与![]() 个数的比值为___________________。
个数的比值为___________________。
(4)FeCl3晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:_______________________________。
(5)氮、磷、砷虽为同主族元素,但其化合物的结构与性质是多样化的。
①该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示,则Y轴可表示的氢化物(RH3)性质可能有________。
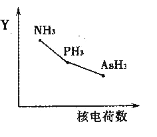
a.稳定性 b.沸点 c.R—H键能 d.分子间作用力
②碳氮化钛化合物在汽车制造和航空航天等领域有广泛的应用,其结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,据此分析,这种碳氮化钛化台物的化学式为______。
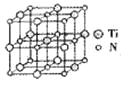
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com