
 如图为2012年第29届伦敦奥运会使用的火炬,火炬中的燃料是丙烷(燃烧热为2221.5kJ/mol).下列正确的是( )
如图为2012年第29届伦敦奥运会使用的火炬,火炬中的燃料是丙烷(燃烧热为2221.5kJ/mol).下列正确的是( )| A. | 丙烷燃烧的过程中,化学能全部转化为热能 | |
| B. | 丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)→3CO2(g)+4H20(g);△H=-2221.5 kJ•mol-1 | |
| C. | 丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)→3CO2(g)+4H20(l);△H=-2221.5 kJ•mol-1 | |
| D. | 1mol丙烷若先分解生成C、H2,然后C、H2再完全燃烧放出的特例小于2221.5kJ |
分析 A.燃烧过程中伴随着发光发热;
B.燃烧热规定生成稳定的化合物,因此产物水应为液体;
C.按燃烧热规定,丙烷的物质的量是1mol,产物是CO2(g)和H20(g),放出2221.5kJ/mol;
D.根据盖斯定律进行分析.
解答 解:A.丙烷燃烧的过程中,化学能主要转化为热能和光能,故A错误;
B.丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)→3CO2(g)+4H20(l);△H=-2221.5 kJ•mol-1,故B错误;
C.按燃烧热规定,丙烷的物质的量是1mol,产物是CO2(g)和H20(g),放出2221.5kJ/mol,因此丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)→3CO2(g)+4H20(l);△H=-2221.5 kJ•mol-1,故C正确;
D.焓变与起始状态有关,与反应的途径无关,因此1mol丙烷若先分解生成C、H2,然后C、H2再完全燃烧放出的热量等于2221.5kJ,故D错误;
故选C.
点评 本题考查了燃烧热和盖斯定律,难度中等,能根据燃烧热的数值写出相应的热化学方程式是关键,同时注意对盖斯定律的掌握.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
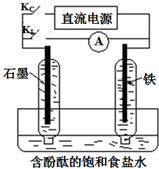 某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )
某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )| A. | 断开KL,闭合KC时,铁作阴极,总反应方程式为2H2O=2H2↑+O2↑ | |
| B. | 断开KL,闭合KC时,石墨电极附近溶液变红 | |
| C. | 断开KC,闭合KL时,石墨作正极,发生还原反应Cl2+2e-=2Cl- | |
| D. | 断开KC,闭合KL时,铁作负极,发生铁的吸氧腐蚀反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
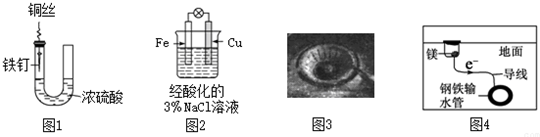
| A. | 图1中,铁钉易生锈 | |
| B. | 图2中,滴加少量K3[Fe(CN)6]溶液,没有蓝色沉淀出现 | |
| C. | 图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 | |
| D. | 图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
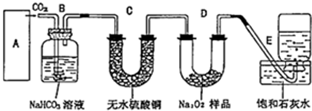 过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出实验装置(如图):
过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出实验装置(如图):查看答案和解析>>
科目:高中化学 来源: 题型:多选题
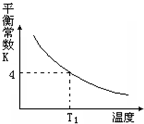 T℃时,将1molX和2molY投入2L的密闭容器中,发生反应:X(g)+Y(g)?2Z(g),X、Y的量随时间变化如下表,该反应的平衡常数随温度的变化如下图,则下列判断正确的是( )
T℃时,将1molX和2molY投入2L的密闭容器中,发生反应:X(g)+Y(g)?2Z(g),X、Y的量随时间变化如下表,该反应的平衡常数随温度的变化如下图,则下列判断正确的是( )| 0 | 1 | 2 | 3 | 4 | 5 | 6 | |
| X | 1 | 0.80 | 0.66 | 0.58 | 0.52 | 0.50 | 0.50 |
| Y | 2 | 1.80 | 1.66 | … | … | … | … |
| A. | 前5min用Z表示的平均反应速率为0.2mol/(L•min) | |
| B. | 该反应的正反应是放热反应,且T1>T | |
| C. | 在T℃时,以1molX、2molY和1molZ充入上述容器中,达到平衡时,X的体积分数不变 | |
| D. | 若温度为T1时,以同样的起始量反应,达到平衡时X的转化率为66.7% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ | |
| B. | 若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ | |
| C. | 若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间不相同 | |
| D. | 平衡时Ⅰ容器的体积小于V L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com