

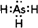 .
.分析 (1)①亚砷酸(H3AsO3)中,氧元素化合价为-2价,氢元素化合价为+1价,结合元素化合价代数和为0计算砷元素的化合价;
②依据同周期变化规律可知,砷酸为弱酸,分步电离;
③“一级沉砷”中FeSO4的作用是除去过量的硫离子提高沉砷效果;
④“二级沉砷”中H2 O2与含砷物质发生氧化还原反应,氧化亚砷酸为砷酸;
⑤流程分析可知钙离子结合硫酸根离子形成硫酸钙沉淀;
(2)①AsH3和氨气分子结构相同为共价化合物,砷原子和三个氢原子形成三个As-H键;
②将AsH3气体通人AgNO3溶液中,生成银镜和As2O3,结合电荷守恒、原子守恒配平书写离子方程式;
③As的最低检出限为3.0x 10 -6g,取1g废渣样品,重复上述实验,未见银镜生成,取10g废渣样品最后生成银镜和As2 O3.则10g废渣含砷量最少为3.0x 10 -6g,据此分析;
解答 解:(1)①亚砷酸(H3AsO3)中,氧元素化合价为-2价,氢元素化合价为+1价,砷元素化合价设为x,+1×3+x+(-2)×3=0,x=+3,
故答案为:+3;
②第ⅤA族非金属元素形成最高价含氧酸中磷、砷形成的含氧酸都是弱酸,水溶液中分步电离,电离方程式为:H3AsO4?H++H2AsO4-,
故答案为:H3AsO4?H++H2AsO4-;
③“一级沉砷”中FeSO4的作用是除去过量的硫离子,As2S3+3S2-?2AsS32-使平衡逆向进行,提高沉砷效果,
故答案为:除去过量的硫离子,As2S3+3S2-?2AsS32-使平衡逆向进行,提高沉砷效果;
④“二级沉砷”中H2 O2与含砷物质发生氧化还原反应,氧化亚砷酸为砷酸;,反应的化学方程式为:H3AsO3+H2O2=H3AsO4+H2O,
故答案为:H3AsO3+H2O2=H3AsO4+H2O;
⑤流程分析可知,加入氧化钙和水反应生成氢氧化钙,氢氧化钙和砷酸反应生成砷酸钙沉淀、和铁离子反应生成氢氧化铁沉淀,钙离子结合硫酸根离子形成硫酸钙沉淀,所以沉淀X为CaSO4,
故答案为:CaSO4;
(2)①AsH3和氨气分子结构相同为共价化合物,砷原子和三个氢原子形成三个As-H键,电子式为: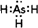 ,
,
故答案为: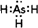 ;
;
②将AsH3气体通人AgNO3溶液中,生成银镜和As2O3,结合电荷守恒、原子守恒配平书写离子方程式为:12Ag++2AsH3+3H2O=12Ag↓+As2O3+12H+,
故答案为:12Ag++2AsH3+3H2O=12Ag↓+As2O3+12H+;
③As的最低检出限为3.0x 10 -6g,取1g废渣样品,重复上述实验,未见银镜生成,取10g废渣样品最后生成银镜和As2 O3.则10g废渣含砷量最少为3.0x 10 -6g,含砷量大于3.0×10-4g/kg>4.0×10一5g•kg-1,不符合排放标准,
故答案为:该废渣中砷元素含量超过3.0×10-4g/kg,不符合排放标准;
点评 本题考查了废水处理方法和构成、物质性质分析、氧化还原反应实质理解、离子方程式书写等知识点,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
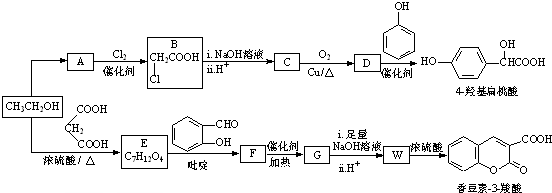
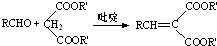 (R,R′,R″表示氢、烷基或芳基)
(R,R′,R″表示氢、烷基或芳基)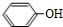 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$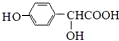 .
.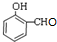 $\stackrel{吡啶}{→}$
$\stackrel{吡啶}{→}$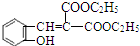 +H2O.
+H2O.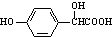 )的同分异构体
)的同分异构体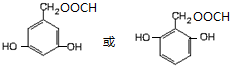 .
.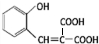 $\stackrel{浓硫酸}{→}$
$\stackrel{浓硫酸}{→}$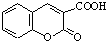 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
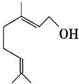 香叶醇是合成玫瑰香油的主要原料,结构可用键线式表示如图,键线式中每个端点和拐点处都代表有一个碳原子,氢原子可根据碳为四价的原则而相应地在碳上补充.下列有关香叶醇的叙述正确的是( )
香叶醇是合成玫瑰香油的主要原料,结构可用键线式表示如图,键线式中每个端点和拐点处都代表有一个碳原子,氢原子可根据碳为四价的原则而相应地在碳上补充.下列有关香叶醇的叙述正确的是( )| A. | 香叶醇的分子式为C10H18O | B. | 不能使溴的四氯化碳溶液褪色 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 能发生加成反应不能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
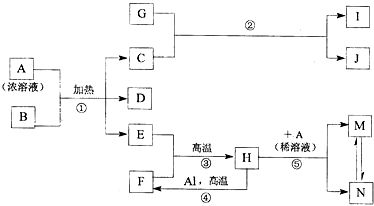
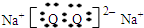 ,化合物J的俗名纯碱.
,化合物J的俗名纯碱.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
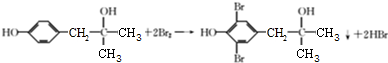
 +Br2
+Br2
 .
.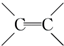 $\stackrel{稀,冷KMnO_{4},溶液/OH-}{→}$
$\stackrel{稀,冷KMnO_{4},溶液/OH-}{→}$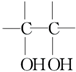 .请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式
.请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式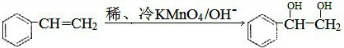 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2015年中国诺贝尔生理学奖获奖者屠呦呦女士用乙醚从黄花蒿中提取青蒿素,该技术应用了分馏原理 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 生物炼铜原理是利用某些具有特殊本领的细菌把不溶性的硫化铜转化为铜单质 | |
| D. | 近日我国科学家成功制得反应物--超快正电子,正电子与负电子相遇就会湮灭并释放出极大的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 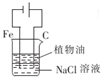 用图装置制取Fe(OH)2沉淀 | B. | 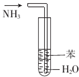 用图装置吸收NH3并防止倒吸 | ||
| C. | 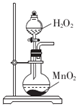 用图装置制取少量氧气 | D. | 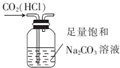 用图装置除去CO2中含有的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

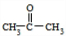 .
.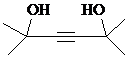 .
. .
.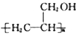 的合成路线图(无机试剂任用).合成路线图示例如下:
的合成路线图(无机试剂任用).合成路线图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
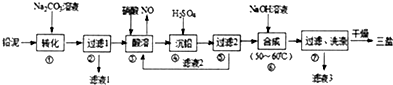
| A. | 步級①PbSO4转化为难溶PbCO3的离子方程式为CO32-+PbSO4=PbCO3+SO42- | |
| B. | 步骤③酸溶时,PbO、Pb、PbCO3都与硝酸反应生成Pb(NO3)2; 滤液2中可回收再利用的主要成分为HNO3 | |
| C. | 滤液1、滤液3中所含的溶质完全相同 | |
| D. | 步骤⑥合成三盐的化学方程式为4PbSO4+6NaOH=3Na2SO4+3PbO•PbSO4•H2O+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com