
【题目】在饱和Mg(OH)2溶液中,c(OH-)=1.0×10-4 mol·L-1。若往该溶液中加入NaOH溶液,使溶液的c(OH-)变为原来的10倍,则Mg(OH)2的溶解度在理论上将
A.变为原来的10-3倍 B.变为原来的10-2倍
C.变为原来的10倍 D.不发生变化
科目:高中化学 来源: 题型:
【题目】12mL浓度为0.10molL-1的Na2SO3溶液,恰好与10mL浓度为0.04molL-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
A. +5
B. +4
C. +3
D. +2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种烃,其球棍模型如图:
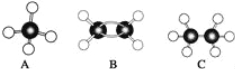
(1)等质量的以上物质完全燃烧时耗去O2的量最多的是 (填对应字母,下同)。
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是 。
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是 。
(4)在120℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物品或设备:
①陶瓷餐具 ②砖瓦③水泥路桥 ④门窗玻璃⑤水晶镜片 ⑥石英钟表⑦玛瑙手镯 ⑧硅太阳电池⑨光导纤维 ⑩计算机芯片
(1)用到硅单质的是 .
(2)所用材料为SiO2或要用到SiO2的是
(3)所用材料为硅酸盐的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应在任何温度下均能自发进行的是( )
A. 2N2(g)+O2(g)═2N2O(g)△H=+163kJmol1 B. Ag(s)+1/2Cl2(g)═2AgCl(s)△H=127kJmol1 C. 2HgO(s)═2Hg(l)+O2(g)△H=+91kJmol1 D. 2H2O2(l)═O2(g)+2H2O(l)△H=98kJmol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极分别电解下列各物质的水溶液一段时间后,向剩余溶液中加入适量水能使溶液恢复到电解前浓度的是
A.AgNO3 B.NaCl C.CuCl2 D.H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
PET是世界上产量最大的合成纤维,其结构简式为:
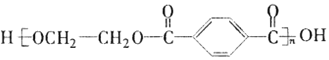
现以煤的干馏产品A与F为原料制备PET,生产的工艺流程如图所示。
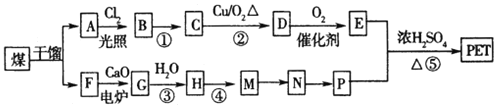
其中A为烃,含碳元素的质最分数为90.6%,其蒸气密度是空气密度的3.66倍,且能使酸性高锰酸钾溶液褪色,但不能使溴水褪色。M分子里所有原子共平面。
请回答下列问题:
(1)A的名称为______。M→N的反应类型为______ ;
(2)反应①的反应条件为:______;
(3)写出有机物A所有一氯代物的结构简式:______。
(4)写出下列反应的化学方程式:
反应②:_________;反应③:_________。D与足量的氢氧化铜悬浊液煮沸:_________;
反应⑤:_________。
(5)P的一种同系物X的分子式为C3H8O2,在核磁共振氢谱图中出现三种信号峰,其峰的强度之比为2:l : l 。则X的结构简式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将30ml 0.5mol/L NaOH溶液稀释到500ml,稀释后取出5ml,则溶液中NaOH的物质的量浓度为 ( )
A. 0.03mol/L B. 0.3mol/L C. 0.05mol/L D. 0.04mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业采用氯化铵焙烧菱锰矿制备碳酸锰的流程如下图所示:
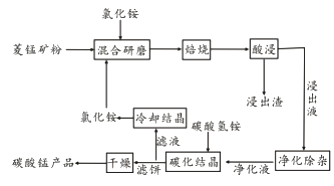
已知:①菱锰矿的主要成分是MnCO3 ,其中含Fe、Ca、Mg、Al等元素。
②焙烧过程中主要反应为:MnCO3 +2NH4Cl ![]() MnCl2+2NH3↑ +CO2↑+ H2O。
MnCl2+2NH3↑ +CO2↑+ H2O。
③部分阳离子沉淀时溶液的pH的值:
Al3- | Fe3+ | Ca2+ | Mn2+ | Mg2+ | |
开始沉淀的pH值 | 4.1 | 2.2 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH值 | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
(1)实验室“焙烧”操作盛放固体的仪器为____________________。
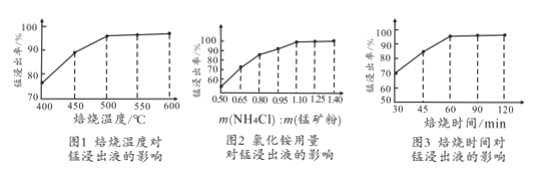
(2)结合图1、2、3,分析焙烧过程中对温度、NH4Cl用量[m(NH4Cl):m(锰矿粉)]、时间的最佳选择依次为________________、_______________、______________。
(3)对锰浸出液净化除杂时,先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围为_________________,将Fe3+和Al3+变为沉淀除去。然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(4)“碳化结晶”步骤中,加入碳酸氢铵是反应的离子方程式为________________。
(5)上述流程中可循环使用的物质是_______________。
(6)为测定产品中碳酸锰的含量,设计如下实验(杂质不参加反应):实验步骤为:称取16.80g试样,溶于适量的稀硫酸溶液中,向所得溶液中加入稍过量的磷酸和硝酸,加热使反应:2Mn2++NO3-+4PO43-+2H+![]() 2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+,滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+,滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为_____________________(还原产物是Cr3+。
②产品中碳酸锰的质量分数为_____________(结果保留3位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com