
某温度下,V mL不饱和NaNO3溶液a g,蒸发掉b g水或加入b g NaNO3固体(恢复到原温度)均可使溶液达到饱和,则下列量的计算结果正确的是
A.该温度下NaNO3的溶解度为200 g
B.原不饱和溶液中NaNO3的质量分数为 %
%
C.原不饱和溶液中NaNO3的物质的量浓度为 mol/L
mol/L
D.原不饱和溶液的密度为 g/mL
g/mL
C
【解析】
试题分析:A、蒸发掉b g水或加入b gNaNO3固体(恢复到原温度)均可使溶液达到饱和,说明一定温度下bgNaNO3固体溶于bg水中形成的是饱和溶液,根据溶解度概念列式计算设溶解度为S,则=100g,故该温度下NaNO3的溶解度为100g,故A错误;B、设不饱和溶液中溶质为xg,蒸发水bg后为饱和溶液,溶解度为100g,则依据溶解度概念列式计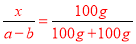 ,解得x=
,解得x=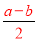 ,所以原不饱和溶液中NaNO3质量分数
,所以原不饱和溶液中NaNO3质量分数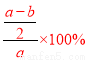 =
=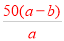 %,B错误;设不饱和溶液中溶质为xg,蒸发水bg后为饱和溶液,溶解度为100g,则依据溶解度概念列式计算
%,B错误;设不饱和溶液中溶质为xg,蒸发水bg后为饱和溶液,溶解度为100g,则依据溶解度概念列式计算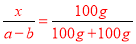 ,x=
,x=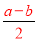 ,原不饱和溶液中NaNO3物质的量浓度
,原不饱和溶液中NaNO3物质的量浓度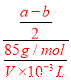 =
=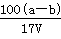 mol/L,C正确;溶液的密度=
mol/L,C正确;溶液的密度=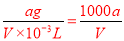 g/L,D错误,答案选C。
g/L,D错误,答案选C。
考点:溶解度的概念及应用


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学文科试卷(解析版) 题型:填空题
(10分)下列是元素周期表的中的部分元素,请回答。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中所标出的元素当中,最活泼的金属元素是 ;常用作半导体材料的硅元素是 ,它的最高价氧化物的化学式是 。
(2)向污水中加入含有元素⑦的 (填名称,下同)做混凝剂,可以使水中的悬浮颗粒物沉降;元素⑨的单质与水反应的产物 具有强氧化性,可杀死水中的细菌。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学理科试卷(解析版) 题型:选择题
在一定温度下的定容密闭容器中,当下列物理量不再改变时,不能表明反应A(s)+2B(g) C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.混合气体的相对分子质量 D.C气体的总物质的量浓度
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省师大一附高一上学期期中化学试卷(解析版) 题型:实验题
(14分)用密度为1.84g/mL,质量分数为98%的浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释 ④转移
⑤洗涤 ⑥定容 ⑦摇匀
(1)所需浓硫酸的体积是 。
(2)第③步实验的操作是 。
(3)第⑥步实验的操作是 。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用字母填写a.偏大 b.偏小 c.无影响)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.量取浓硫酸时仰视量筒上的刻度取用浓硫酸
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
F.把配好的溶液倒入用蒸馏水洗净而未干的试剂瓶中备用
(5)本实验最浪费时间的地方是将稀释后的硫酸冷却至室温,为了节约时间,简单易行的加
快稀硫酸冷却的方法是_______________________________________.
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省师大一附高一上学期期中化学试卷(解析版) 题型:选择题
分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
①根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④根据反应物、生成物种类和类别将化学反应分为化合、分解、置换、复分解四大基本反应
A.①② B.③④ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省师大一附高一上学期期中化学试卷(解析版) 题型:选择题
某氯化镁溶液的密度为1.6g·cm-3,其中镁离子的质量分数为5 %,300mL该溶液中Cl-离子的物质的量约等于
A.0.37 mol B.0.63mol C.2 mol D.1.5mol
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高一上学期期中化学试卷(解析版) 题型:实验题
(11分)过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 == 2Na2CO3 + O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:

(1)A中制取CO2 的装置,应从下列图①和②中选哪个图:

B装置的作用是 ,C装置内出现的现象是 。为了检验E中收集到的气体,在取出集气瓶后,用 的木条伸入集气瓶内,木条会出现 。
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因: 。
(3)反应完毕时,若测得E中的集气瓶收集到的气体250毫升,又知氧气的密度为1.43克/升,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值 (偏大或偏小),相差约 毫升(取整数值,所用数据均在标准状况下测定),这可能是由于 。
(4)你认为上述A---E的实验装置中,E部分是否安全、合理?
E是否需要改进,若需要改进,应改为下图中的 (填甲、乙、丙、丁).

查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高一上学期期中化学试卷(解析版) 题型:选择题
关于胶体和溶液的区别,下列叙述中正确的是
A.溶液是透明的,胶体是不透明的
B.溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
C.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明显光带
D.溶液稳定,放置后不会生成沉淀,胶体不稳定,放置会生成沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期第四次月考理综化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.标准状况下,11.2L苯中含有分子的数目为0.5NA
B.0.1mol丙烯酸中含有双键的数目为0.1NA
C.1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
D.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com