
| A、已知甲烷的燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═2CO2(g)+2H2O(g)△H=-890.3 kJ?mol-1 |
| B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C、已知中和热为△H=-57.4 kJ?mol-1,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热 |
| D、已知S(g)+O2(g)═SO2(g)△H1; S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 |


科目:高中化学 来源: 题型:
| A、配制一定物质的量浓度的溶液时,定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水到刻度 |
| B、锥形瓶盛装待测液前需先用蒸馏水洗净,再用待测液润洗 |
| C、石蕊试纸在测定气体酸碱性时必须用蒸馏水润湿 |
| D、向稀氢氧化钠溶液中滴加饱和氯化铁溶液并不断搅拌,制取氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、在蒸发皿中灼烧CuSO4?5H2O晶体以除去结晶水 |
| B、配制0.1 mol?L-1硫酸溶液时,容量瓶应先用0.1 mol?L-1硫酸溶液润洗 |
| C、用图a所示装置实验,振荡后静置,溶液不再分层,且保持无色透明 |
| D、实验室用图b所示装置制取少量的氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol乙酸和1mol乙醇充分反应生成的水分子数为NA |
| B、常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA |
| C、标准状况下,2.24L的CCl4中含有的C-Cl键数为0.4NA |
| D、6.8g液态KHSO4中含有0.1NA个阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- |
| B、NaHCO3溶液中:c(HCO3-)+c(H2CO3)+c(CO32-)=c(Na+) |
| C、相同温度下,10 mL0.1 mol?L-1的醋酸与100 mL0.01mol?L-1的醋酸中的H+物质的量不相等 |
| D、中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
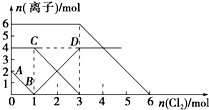 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )| A、线段BD表示Fe3+物质的量的变化 |
| B、原混合溶液中FeBr2的物质的量为3mol |
| C、当通入2mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
| D、原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳和水反应吸收131.3 kJ能量 |
| B、1 mol碳和1 mol水反应生成1 mol一氧化碳和1 mol氢气并吸收131.3 kJ热量 |
| C、1 mol固态碳和1 mol水蒸气反应生成1 mol一氧化碳气体和1 mol氢气并吸收131.3 kJ热量 |
| D、1个固态碳原子和1分子水蒸气反应吸热131.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
c(N
| ||
| c(NH3?H2O) |
| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com