
铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与5.6 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。则消耗铜的质量为( )
A.16 g B.32 g
C.64 g D.无法计算
★ ★★
科目:高中化学 来源: 题型:
不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如图所示。
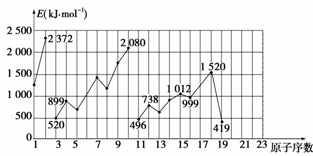
试根据元素在同期表中的位置,分析图中曲线的变化特点,并回答下列问题。
(1)同主族内不同元素的E值变化的特点是_________________________________。各主
族中E值的这种变化特点体现了元素性质的____________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系式中正确的是________(填写编号,多选倒扣)。
①E(砷)>E(硒) ②E(砷)<E(硒)
③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1 mol气态Ca原子失去最外层一个电子所需能量E值的范围:
_____<E<____________。
(4)10号元素E值较大的原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
答案 AB
解析 水分子中各原子已达到稳定结构,H3O+是H+和H2O中的O形成配位键;[B(OH)4]-是3个OH-与B原子形成3个共价键,还有1个OH-的O与B形成配位键;其他项均不能形成配位键。
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
答案 A
解析 反应过程①+②得O2—→2O,③O+O2—→O3,NO2起催化剂作用,反应过程中NO2作氧化剂,A项正确,B、C项错误;O3与O2的相对分子质量不相同,不是同分异构体,属同素异形体,D项错误。
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3是一种重要的化工原料,可以制备一系列物质(如图)。下列有关表述正确的是( )
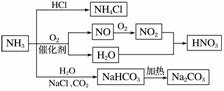
A.NH4Cl和NaHCO3都是常用的化肥
B.NH4Cl、HNO3和Na2CO3受热时都易分解
C.NH3和NO2在一定条件下可发生氧化还原反应
D.图中所涉及的盐类物质均可以水解
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
一定质量的铁和足量的稀硝酸或浓硝酸完全反应,在相同条件下,用排水集气法收集产生的气体。下列叙述一定正确的是( )
①硝酸浓度越大,消耗的硝酸越少
②硝酸浓度不同,生成的Fe(NO3)3的物质的量相同
③硝酸浓度越大,产生的气体越少
④用排水集气法收集到的气体在相同状况下体积相同
A.只有② B.②④ C.③④ D.①②③
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z是三种主族元素,如果Xn+阳离子与Yn-阴离子具有相同的电子层结构,Zn-阴离子半径大于Yn-阴离子半径,则三种元素的原子序数由大到小的顺序是( )
A.Z>X>Y B.X>Y>Z
C.Z>Y>X D.X>Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列叙述,写出元素名称和核外电子排布式。
(1)A元素原子核外M层电子数是L层电子数的一半:___________。
(2)B元素原子的最外层电子数是次外层电子数的1.5倍:________________。
(3)C元素的单质在常温下可与水剧烈反应,产生的气体能使带火星的木条复燃:________________________________________。
(4)D元素的次外层电子数是最外层电子数的1/4:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com