
| A. | 金刚石>晶体硅>二氧化硅>碳化硅 | B. | I2>Br2>Cl2>F2 | ||
| C. | H2Te>H2Se>H2S>H2O | D. | 金刚石>CsCl>NaCl>钠 |
分析 A.原子晶体中共价键的键长越短,键能越大,熔、沸点越大;
B.卤族元素中,原子序数越大,单质的熔沸点越高;
C.水分子间存在氢键;
D.离子晶体的熔沸点与电荷成正比、与离子半径成反比.
解答 解:A.原子晶体中共价键的键长越短,键能越大,熔、沸点越大,则熔、沸点为金刚石>二氧化硅>碳化硅>晶体硅,故A错误;
B.卤素单质中,原子序数越大,对应单质的熔沸点越大,则熔沸点大小为:I2>Br2>Cl2>F2,故B正确;
C.水分子间存在氢键,所以熔沸点高低顺序是H2O>H2Te>H2Se>H2S,故C错误;
D.离子晶体中,熔沸点与电荷成正比、与离子半径成反比,钠离子、铯离子和氯离子都带一个单位电荷,且铯离子半径大于钠离子,则熔沸点NaCl>CsCl,故D错误;
故选B.
点评 本题考查常见物质熔沸点高低判断,题目难度不大,明确晶体类型及晶体熔沸点高低影响因素即可解答,试题培养了学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:实验题
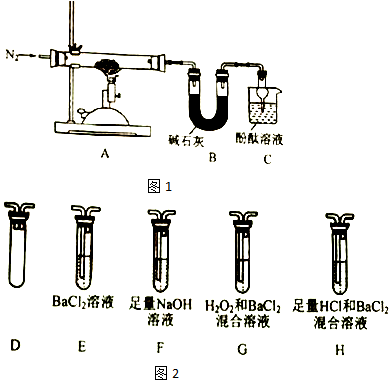
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H、Be、B 原子最外层电子数依次增多 | |
| B. | P、S、Cl 元素最高正化合价依次升高 | |
| C. | F2、Cl2、Br2、I2的熔点依次降低 | |
| D. | Li、Na、K、Rb的金属性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸溶液导电性比乙酸溶液导电性强,说明乙酸是弱酸 | |
| B. | 硫酸钾溶于水能导电,所以硫酸钾是电解质 | |
| C. | 强电解质一定是含有离子键,弱电解质中一定含弱极性共价键 | |
| D. | 固态磷酸是电解质,所以磷酸在熔融状态下和水溶液中都能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑的现象,说明浓硫酸具有脱水性 | |
| B. | Na的金属活动性比Mg强,说明可用Na与MgCl2溶液反应制Mg | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸反应生成了致密的氧化物 | |
| D. | 向碘水中滴加CCl4,振荡静置后分层,下层呈紫红色,说明可用CCl4从碘水中萃取碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、H2的浓度之比保持不变 | |
| B. | N2和H2的反应速率之比为1:3 | |
| C. | NH3的生成速率与H2的生成速率之比为2:3 | |
| D. | 体系中N2、H2、NH3的分子个数之比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:5 | B. | 1:4 | C. | 3:2 | D. | 5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com