
现有浓度0.1 mol·L-1的五种电解质溶液①NA2CO3 ②NAHCO3 ③NAAlO2 ④CH3COONA ⑤NAOH
已知:CO2+3H2O+2![]() ====2Al(OH)3↓+
====2Al(OH)3↓+![]()
(1)这五种溶液的pH由小到大的顺序是_______________(填编号)。
(2)将五种溶液稀释相同的倍数时,其pH变化最大的是_______________(填编号)。
(3)在上述五种溶液中分别加入AlCl3溶液,能产生无色无味气体的是_______(填编号)。
(4)将上述①②③④四种溶液两两混合时,有一对溶液相互间能发生反应,写出该反应的离子方程式:
_____________________________________________________________________。
(1)④②①③⑤(2)⑤(3)①②(4)![]() +
+![]() +H2O====Al(OH)3↓+
+H2O====Al(OH)3↓+![]()
本题指明①浓度相同0.1 mol·L-1 ②CO2+2![]() +3H2O====2Al(OH)3↓+
+3H2O====2Al(OH)3↓+![]()
(1)酸性越弱,其盐水解程度越大,pH越大。则pH由小到大的顺序是④②①③⑤,即CH3COONa<NaHCO3<Na2CO3<NaAlO2<NaOH
相同的多元弱酸,其酸式盐的水解程度小于正盐的水解程度。(2)稀释相同的倍数,则NaOH的pH变化最大,因为NaOH完全电离。
(3)与AlCl3反应的有①②③⑤,但能产生气体的是①②。
2Al3++3![]() +3H2O====2Al(OH)3↓+3CO2↑
+3H2O====2Al(OH)3↓+3CO2↑
Al3++3![]() ====Al(OH)3↓+3CO2↑
====Al(OH)3↓+3CO2↑
Al3++3![]() +6H2O====4Al(OH)3↓
+6H2O====4Al(OH)3↓
(4)两两混合能反应的是NaHCO3和NaAlO2。
![]() +
+![]() +H2O====Al(OH)3↓+
+H2O====Al(OH)3↓+![]()


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
| A、反应温度10°,Na2S2O3体积5ml,浓度0.2/mol?L-1,H2SO4体积5ml,浓度0.1/mol?L-1,H2O体积10mL | B、反应温度10°,Na2S2O3体积5ml,浓度0.1/mol?L-1,H2SO4体积5ml,浓度0.1/mol?L-1,H2O体积10mL | C、反应温度30°,Na2S2O3体积5ml,浓度0.1/mol?L-1,H2SO4体积5ml,浓度0.1/mol?L-1,H2O体积10mL | D、反应温度30°,Na2S2O3体积5ml,浓度0.2/mol?L-1,H2SO4体积5ml,浓度0.2/mol?L-1,H2O体积10mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO2+3H2O+2![]() ====2Al(OH)3↓+
====2Al(OH)3↓+![]()
(1)这五种溶液的pH由小到大的顺序是_______________(填编号)。
(2)将五种溶液稀释相同的倍数时,其pH变化最大的是_______________(填编号)。
(3)在上述五种溶液中分别加入AlCl3溶液,能产生无色无味气体的是_______(填编号)。
(4)将上述①②③④四种溶液两两混合时,有一对溶液相互间能发生反应,写出该反应的离子方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO2+3H2O+2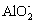 ══2Al(OH)3↓+CO
══2Al(OH)3↓+CO![]()
(1)这五种溶液的pH由小到大的顺序是:________(填编号)。?
(2)将五种溶液稀释相同的倍数时,其pH变化最大的是:________(填编号)。?
(3)在上述五种溶液中分别加入AlCl3溶液,能产生无色无味气体的是:________(填编号)。
(4)将上述①②③④四种溶液两两混合时,有一对溶液相互间能发生反应,写出该反应的离子方程式: 。?
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省嘉兴一中高一10月份月考化学试卷 题型:实验题
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题: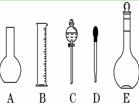
(1)如图 所示的仪器中配制溶液肯定不需要的是 (填序号),
所示的仪器中配制溶液肯定不需要的是 (填序号),
仪器C的名称是 ,
本实验所需玻璃仪器E规格为 mL。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度 的标准溶液 的标准溶液 | B.长期贮存溶液 |
| C.用来加热溶解固体溶质 | D.量取一定体积的液体 |
 留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。
留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com