
高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性。
(1)已知:4FeO42-+10H2O  4Fe(OH)3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有 。
4Fe(OH)3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有 。
同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH= 的溶液。
(2)高铁酸钾有以下几种常见制备方法:
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 电解法 | 制备中间产物Na2FeO4,再与KOH溶液反应 |
①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为____ 。
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式: 。
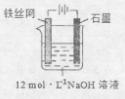
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应
式为 。
(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:
3Zn+2K2FeO4+8H2O  3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
放电时负极材料为 ,正极反应为: 。
(4) 25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L,含有2.0×l0-4 mol·L-l K2FeO4的废水中有CaFeO4沉淀产生,理论上至少加入Ca(OH)2的物质的量为 mol。
【知识点】氧化还原反应规律、电化学、难溶物的沉淀溶解平衡 B3 F3 H5
【答案解析】(1)K2FeO4具有强氧化性,能够消毒杀菌;同时FeO42- 被还原成Fe3+,Fe3+水解形成Fe(OH)3胶体,能够吸附水中悬浮杂质。11.50
(2)
①3:1(2分)
② 2FeO42-+Fe3++8OH-=3FeO43-+4H2O(2分)
③Fe+8OH--6e─=FeO42─+4H2O(2分)
(3)Zn(1分) FeO42-+4H2O+3e-== Fe(OH)3+5OH-(2分)
(4)2.27×10-2(2分)
解析:(1)所给方程式体现了K2FeO4具有强氧化性,能够消毒杀菌,同时FeO42- 被还原成Fe3+;结合胶体的性质想到第二点:Fe3+水解形成Fe(OH)3胶体,能够吸附水中悬浮杂质。 根据反应方程式可知酸会促进K2FeO4水解,而碱会抑制K2FeO4水解,所以在碱性强的溶液中能稳定存在。
(2)
①反应Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O中,Fe元素化合价升高,化合价由+3价升高到+6价被氧化,N元素化合价由+5价降低到+2价,氧化剂与还原剂的物质的量之比为3:1,
② 根据提示:2FeO42-+Fe3++8OH-=3FeO43-+4H2O
③制备中间产物Na2FeO4利用电解法,结合阳极发生氧化反应得:Fe+8OH--6e─=FeO42─+4H2O
(3)放电时为原电池,锌的化合价升高锌做负极;正极发生的电子的反应: FeO42-+4H2O+3e-== Fe(OH)3+5OH-
(4)至少加入Ca(OH)2的物质的量为: =2.27×10-2(mol)
=2.27×10-2(mol)
【思路点拨】本题考查了氧化还原反应规律、电化学、难溶物的沉淀溶解平衡,注意根据题目提示进行分析解答。


科目:高中化学 来源: 题型:
根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=﹣Q1 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(l)△H=﹣Q2 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(g)△H=﹣Q3 kJ/mol
判断Q1、Q2、Q3三者关系正确的是( )
|
| A. | Q1>Q2>Q3 | B. | Q1>Q3>Q2 | C. | Q3>Q2>Q1 | D. | Q2>Q1>Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铁是人类较早使用的金属之一.运用铁及其化合物的知识,完成下列问题.
(1)所含铁元素既有氧化性又有还原性的物质是 (用字母代号填).
A.Fe; B.FeCl3; C.FeSO4; D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是 nm.
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式: .某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是 ,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05g.溶液中c(Cl﹣)= mol/L.
(4)若要验证该溶液中含有Fe2+,正确的实验方法是B.
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+;
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+;
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+.
(5)欲从废水中回收铜,并重新获得FeCl3溶液设计实验方案如下:
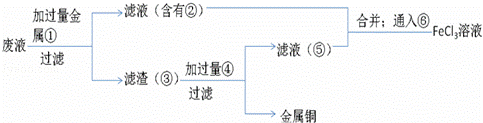
A.请写出上述实验中加入或生成的有关物质的化学式:
① ;② ;③ ;④HCl.
B.请写出通入⑥的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质中可能有甲醇、甲酸、乙醇、甲酸乙酯几种物质中的一种或几种,在鉴定时有下列现象:①有银镜反应 ②加入新制Cu(OH)2悬浊液,沉淀不溶解,③与含有酚酞的NaOH溶液共热时发现溶液中红色逐渐变浅至无色,下列叙述中正确的是( )
|
| A. | 一定有甲酸乙酯和甲酸 |
|
| B. | 一定有甲酸乙酯和乙醇 |
|
| C. | 一定有甲酸乙酯,可能有甲醇 |
|
| D. | 几种物质都一定有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A分子的结构简式为: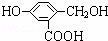
(1)A跟NaOH溶液反应的化学方程式是: ;
(2)A跟NaHCO3溶液反应的化学方程式是: ;
(3)A在一定条件下跟Na反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
B、CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)增大
C、Ca(HCO3)2溶液与过量NaOH溶液反应可制得Ca(OH)2
D、25℃时Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度
查看答案和解析>>
科目:高中化学 来源: 题型:
某容器中充入H2和N2,在一定条件下合成NH3,下列叙述不正确的是( )
A.开始反应时,正反应的速率最大
B.随着反应的进行,正反应的速率逐渐减小,最终减小为零
C.随着反应的进行,逆反应的速率逐渐增大,后保持不变
D.随着反应的进行,正反应的速率逐渐减小,最终与逆反应的速率相等且保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液一定显酸性的是( )
A.溶液中[OH-]>[H+]
B.滴加紫色石蕊试液后变红色的溶液
C.溶液中[H+]=10-6 mol·L-1
D.pH<7的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com