
从1L1mol/LNaOH溶液中取出100ml,下列关于这100ml溶液的叙述中错误的是( )
|
| A. | 含NaOH0.1mol | B. | 浓度为1mol/L | C. | 含NaOH4g | D. | 浓度为0.1mol/L |
| 物质的量浓度.. | |
| 专题: | 物质的量浓度和溶解度专题. |
| 分析: | A、根据n=CV计算判断. B、D从一定体积的溶液中取出部分溶液,部分溶液的浓度不变. C、m=CVM计算溶质的质量. |
| 解答: | 解:A、n=CV=1mol/×0.1L=0.1mol,故A正确. B、从一定体积的溶液中取出部分溶液,部分溶液的浓度不变,所以这100mL溶液的物质的量浓度为1mol/L,故B正确. C、m=CVM=1mol/×0.1L×40g/mol=4g,故C正确. D、从一定体积的溶液中取出部分溶液,部分溶液的浓度不变,所以这100mL溶液的物质的量浓度为1mol/L,故D错误. 故选D. |
| 点评: | 本题考查了有关物质的量浓度的计算,难度不大,明确从一定体积的溶液中取出部分溶液,部分溶液的浓度不变. |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列物质中,含有0.4mol氯离子的是( )。
A. 0.4mol KClO3 B. 4/30 mol FeCl3 C. 3/40 mol FeCl3 D. 0.1mol KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
与171g Al2(SO4)3中所含的SO42-数目相同的Na2SO4的质量是多少?将171g Al2(SO4)3和142g Na2SO4混合,其混合物的平均摩尔质量是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质按酸、碱、盐分类顺次排列的是( )
|
| A. | 硫酸(H2SO4)、纯碱(Na2CO3)、食盐(NaCl) |
|
| B. | 硝酸(HNO3)、烧碱(NaOH)、胆矾(CuSO4•5H2O) |
|
| C. | 醋酸(CH3COOH)、乙醇(C2H5OH)、硫酸铵((NH4)2SO4) |
|
| D. | 盐酸(HCl)、熟石灰(Ca(OH)2)、苛性钠(NaOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 标准状况下,6.02×1023个分子所占的体积约是22.4L |
|
| B. | 0.5molH2所占体积为11.2L |
|
| C. | 标准状况下,1mol水的体积为22.4L |
|
| D. | 标准状况下,28gCO与N2的混和气体的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 纯碱、烧碱均属碱 |
|
| B. | CO、SO2均属酸性氧化物 |
|
| C. | 凡能电离出H+的化合物均属酸 |
|
| D. | 盐类物质一定含有金属离子或铵根离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气里含有的NO气体是由内燃机燃烧时产生的高温引起氮气和氧气反应所致:N2(g)+O2(g)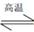 2NO(g)
2NO(g) 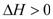
已知该反应在 2404℃时,平衡常数 K=6.4×10-3。请回答下列问题。
2404℃时,平衡常数 K=6.4×10-3。请回答下列问题。
(1)该反应的平衡常数表达式为 。
(2)该温度下,向 2 L 密闭容器中充入 N2 和 O2 各 1 mol,平衡时,N2 的转化率是 %(保留整数)。
(3)该温度下,某时刻测得容器内 N2、O2、NO的浓度分别为2.5×10-1mol·L-1、4.0×10-2mol·L-1和3.0×10-3mol·L-1,此时反应________(填“处于化学平衡状态”、“向正方向进行”或“向逆方向进行”),理由是_______。
(4)将 N2、O2 的混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是_________。
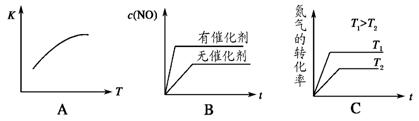
(5)向恒温恒容的密闭容器中充入等物质的量的 N2 和 O2,达到平衡状态后再向其中充入一定量 NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数_________(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于酸、碱、盐中元素组成的说法正确的是
A.酸、碱一定含氢,盐一定不含氧 B.酸、碱、盐可以不含金属元素
C.碱、盐可能含氧,酸一定含氧 D.盐一定含金属元素,酸、碱一定含氧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com