
【题目】根据键能数据(H—Cl 431 kJ/mol,H—I 297 kJ/mol),可得出的结论是 ( )
A. 溶于水时,HI比HCl更容易电离,所以氢碘酸是强酸
B. HI比HCl熔、沸点高
C. HI比HCl稳定
D. 拆开等物质的量的HI和HCl,HI消耗的能量多
科目:高中化学 来源: 题型:
【题目】利用海水可以提取溴和镁,提取过程如下:
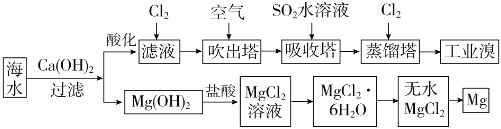
(1)提取溴的过程中,经过2次![]() 转化的目的是__________,吸收塔中发生反应的离子方程式是
转化的目的是__________,吸收塔中发生反应的离子方程式是![]() ,蒸馏塔中发生反应的离子方程式是____________。
,蒸馏塔中发生反应的离子方程式是____________。
(2)从![]() 溶液中得到
溶液中得到![]() 晶体的主要操作是__________、_________、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是__________。
晶体的主要操作是__________、_________、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是__________。
(3)据上述流程,将![]() 海水中溴元素(海水中
海水中溴元素(海水中![]() 离子含量为
离子含量为![]() )转化为工业溴,整个流程中至少需要标准状况下
)转化为工业溴,整个流程中至少需要标准状况下![]() 的体积为_________L(忽略
的体积为_________L(忽略![]() 溶解)。
溶解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.化学反应的焓变与反应的途径有关
B.室温下,稀释0.1mol·L-1CH3COOH溶液,溶液的导电能力减弱
C.常温常压下,22.4L Cl2中含有的分子数为6.02×1023个
D.等质量的铜按a、b两种途径完全转化为Cu(NO3)2,途径a、b消耗的硝酸一样多

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它。用氧化还原观点分析,这“另一物质”在反应中作
A.氧化剂B.还原剂
C.氧化产物D.还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。
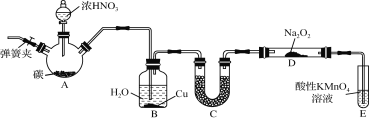
【背景素材】
①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4氧化成NO![]() ,MnO
,MnO![]() 被还原为Mn2+。
被还原为Mn2+。
③在酸性条件下NaNO2能把I-氧化为I2;S2O32-能把I2还原为I-。
【制备NaNO2】
(1) 装置A三颈烧瓶中发生反应的化学方程式为 。
(2) B装置的目的是① ,② 。
(3) 为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是 (填序号)。
A. P2O5 B. 碱石灰 C. 无水CaCl2 D. 生石灰
(4) E装置发生反应的离子方程式是 。
【测定NaNO2纯度】
(5) 本小题可供选择的试剂有:
A.稀硫酸
B.c1mol·L-1KI溶液
C.淀粉溶液
D.c2mol·L-1Na2S2O3溶液
E.c3mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,可选择的试剂是 (填序号)。
②利用NaNO2的氧化性来测定其纯度的步骤是:准确称取质量为m g的NaNO2样品放入锥形瓶中,加适量水溶解 (请补充完整实验步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家成功研发了甲烷和二氧化碳的共转化技术,利用分子筛催化剂高效制得乙酸,下列有关说法正确的是( )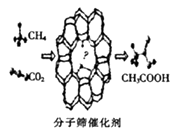
A.消耗22.4 LCO2可制得1mol乙酸
B.该反应过程符合“绿色化学”原理,其原子利用率为100%
C.该反应属于取代反应
D.反应物和生成物中均含有极性键和非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.双原子分子中化学键键能越大,分子越稳定
B.双原子分子中化学键键长越长,分子越稳定
C.双原子分子中化学键键角越大,分子越稳定
D.在双键中,σ键的键能要小于π键的键能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A.红棕色的NO2 , 加压后颜色先变深后变浅
B.高压比常压有利于合成SO3的反应
C.Fe(SCN)3溶液中加入固体KSCN后颜色变深
D.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的工业制法中,正确的是![]()
![]()
A. 制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
B. 制铁:以铁矿石为原料,用焦炭和空气反应生成CO在高温下还原铁矿石中的铁
C. 制镁:用海水为原料,经一系列过程制得氧化镁固体,电解熔融的氧化镁得镁
D. 制钛:用金属钠置换![]() 溶液中的钛
溶液中的钛
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com