
| A. | ②⑤ | B. | ①③④ | C. | ①②③ | D. | ②③④ |
科目:高中化学 来源: 题型:选择题
| A. | 1.0mol•L-1 | B. | 2.0mol•L-1 | C. | 4.0mol•L-1 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
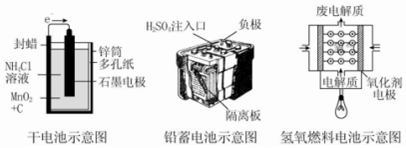
| A. | 上述电池分别属于一次电池、二次电池和燃料电池 | |
| B. | 干电池在长时间使用后,锌筒被破坏 | |
| C. | 氢氧燃料电池是一种具有应用前景的绿色电源 | |
| D. | 铅蓄电池工作过程中,每通过 2 mol 电子,负极质量减轻 207 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 、
、 、
、 .
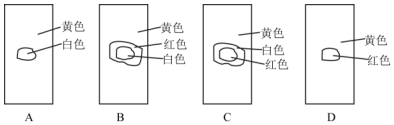
.

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4溶液与Ba(OH)2溶液混合 | B. | NH4Cl溶液与Ca(OH)2溶液混合 | ||
| C. | HNO3溶液与KOH溶液混合 | D. | CH3COOH溶液与NaOH溶液混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雾 | B. | 蛋白质溶液 | C. | 石灰乳 | D. | 硝酸钾溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com