
����Ŀ���Լ״�Ϊԭ����ȡ�ߴ�H2����Ҫ���о����ش��������⣺
��1���״�ˮ��������������Ҫ��������������Ӧ��
����Ӧ��CH3OH(g)��H2O(g)![]() CO2(g)��3H2(g) ��H����49kJ��mol��1
CO2(g)��3H2(g) ��H����49kJ��mol��1
����Ӧ��H2(g)��CO2(g) ![]() CO(g)��H2O(g) ��H����41kJ��mol��1
CO(g)��H2O(g) ��H����41kJ��mol��1
�ټ״��ڴ����������ѽ�ɵõ�H2��CO����Ӧ���Ȼ�ѧ����ʽΪ__________________�����ܼӿ췴Ӧ�����������CH3OHƽ��ת���ʵ�һ�ִ�ʩ��_________________________��
���ʵ�����ˮ����[n(H2O)��n(CH3OH)]�������ڼ״�ˮ�����������⣬������___________��
��ij�¶��£���n(H2O)��n(CH3OH)��1��1��ԭ������������ܱ������У���ʼѹǿΪp1����Ӧ�ﵽƽ��ʱ��ѹǿΪp2����ƽ��ʱ�״���ת����Ϊ_________________�����Ը���Ӧ����
��2����ҵ�ϳ���CH4��ˮ������һ������������ȡH2���䷴Ӧԭ��Ϊ��CH4(g)��H2O(g)![]() CO(g)��3H2(g) ��H����203kJ��mol��1�����ݻ�Ϊ3L���ܱ�������ͨ�����ʵ�����Ϊ3mol��CH4��ˮ��������һ�������·���������Ӧ�����ƽ��ʱH2������������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
CO(g)��3H2(g) ��H����203kJ��mol��1�����ݻ�Ϊ3L���ܱ�������ͨ�����ʵ�����Ϊ3mol��CH4��ˮ��������һ�������·���������Ӧ�����ƽ��ʱH2������������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��

ѹǿΪp1ʱ����N�㣺v��_______v��(����ڡ���С�ڡ����ڡ�)��N���Ӧ�¶��¸÷�Ӧ��ƽ�ⳣ��K��________mol2��L��2��
���𰸡�CH3OH(g)CO(g)��2H2(g) ��H��+90kJ/mol �����¶� ��״���ת���ʣ�������������CO������ ��p2/p1-1����100% ���� 48
��������
��1�����ݸ�˹����ȷ���Ȼ�ѧ����ʽ������������ʽ���м��㣻
��2������ͼ��N�������ƶ���60%ʱ���ﵽƽ��״̬�������ƶ�������ƽ��ʱ�����ʵ�Ũ�ȸ��ݷ���ʽ����K��
��1���ٸ��ݸ�˹���ɣ�����Ӧ+����Ӧ���ɵõ�CH3OH(g)CO(g)��2H2(g) ��H��+90kJ/mol�����CH3OHƽ��ת������Ҫƽ�������ƶ�����ӦΪ���ȷ�Ӧ�������¶ȼ�����߷�Ӧ���ʣ��ֿ���״���ת���ʣ�
���ʵ�����ˮ����[n(H2O)��n(CH3OH)]����ʹ����Ӧ�����ƶ�������CO�����ɣ�����״���ת���ʣ�
�� CH3OH(g)��H2O(g)![]() CO2(g)��3H2(g)
CO2(g)��3H2(g)
��ʼ��1 1
��Ӧ��x x x 3x
ƽ�⣺1-x 1-x x 3x
�ں��¡������ܱ��У�ѹǿ֮�ȵ������ʵ���֮�ȣ�2����2+2x��=p1��p2�����x=p2/p1-1���״���ת����=x/1��100%=��p2/p1-1����100%��
��2������ͼ���֪��ѹǿΪp1ʱ���������������Ϊ60%ʱ����Ӧ�ﵽƽ��״̬�����������������ʵ�������ƽ�������ƶ�����v������v����ƽ��ʱ�������������Ϊ60%����
CH4(g)��H2O(g)![]() CO(g)��3H2(g)
CO(g)��3H2(g)
��ʼ��3 3
��Ӧ��x x x 3x
ƽ�⣺3-x 3-x x 3x
3x/��6+2x��=60%�����x=2��ƽ��ʱ�������ʵ�Ũ�ȷֱ�Ϊ1/3mol/L��1/3mol/L��2/3mol/L��2mol/L��K=2/3��23/��1/3��1/3��=48��


 ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A��ʯ���ѽ�������Ҫ����֮һ������������ں���һ������ʯ�ͻ�����չˮƽ�ı�־���������л���A��G ֮���ת����ϵ��
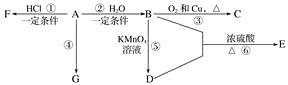
��ش��������⣺
��1��A�Ĺ����ŵ�������_____��C�Ľṹ��ʽ��_____��
��2��E��һ�־�����ζ��Һ�壬��B��D��E�ķ�Ӧ����ʽΪ_______��
��3�������У����˶�Ա������˻�Ť��ʱ�����ҽ���������˲�λ��������F(�е�12.27��)����Ӧ��������д����A��F�Ļ�ѧ����ʽ��________��
��4��E��ͬ���칹������NaHCO3��Һ��Ӧ��д����ͬ���칹��Ľṹ��ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25�桢101kPa�������£�����1 molH��H������436 kJ����������1mol Cl��Cl������243kJ�������γ�1 molH��Cl���ų�431 kJ������
H2��Cl2===2HCl�Ļ�ѧ��Ӧ������ͼ��ʾ��
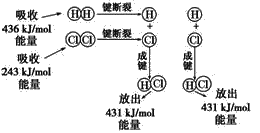
��ش������й����⣺
��1����Ӧ��ϼ����յ�������Ϊ____��
��2��������ɼ��ų���������Ϊ____��
��3��1molH2��1molCl2��Ӧ����2molHCl��_____(���������������ų���)�����ķ�Ӧ��������ֵΪ____��
��4����Ӧ��������___(����>������<��)��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǻ�ˮ������ɵ���ˮ������ˮ����ʱ���������������ߵ��η�(����NaClΪ��)��±֭����ʽ����Χ�ڱ���֮�䣬�γɡ����ݡ�������½ṹ��ͼ��ʾ���������ı���ﵽ1�����ϣ��ڻ����ˮΪ��ˮ������������ȷ����

A.�����ڲ㡰���ݡ��ڵ��η���Ҫ��NaCl���ӵ���ʽ����
B.�����ڲ㡰���ݡ�Խ�࣬�ܶ�ԽС
C.��������Խ�����ڲ�ġ����ݡ�Խ��
D.�������ܶ�Ϊ0.9g��cm��3�����ڲ�NaCl��Ũ��ԼΪ10-4mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0��4gNaOH��1��069![]() ��ϲ������Һ������Һ�еμ�0��1mol��
��ϲ������Һ������Һ�еμ�0��1mol��![]() ϡ���ᡣ����ͼ������ȷ��ʾ������������������
ϡ���ᡣ����ͼ������ȷ��ʾ������������������![]() �����ʵ����Ĺ�ϵ����
�����ʵ����Ĺ�ϵ����
A. B.
B.
C. D.
D.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��1���������ճ������г�����һЩ���ʣ���Һ�ȡ��ھƾ�����CO2������ʯ�ҡ���̼���ơ���ϡ���ᡢ��CaO����Na2O2����Cu������ָ��(��д���)��
���ڼ������������___���ܵ������___��
��2����������ֱ����___nm֮��
��.��ѧ�����ڻ�ѧ��ռ����Ҫ��λ�����ݼ�����գ�
��1��ʵ����ijŨ�������������Ϊ36.5%���ܶ�Ϊ1.20g��cm��3����Ũ��������ʵ���Ũ����___mol��L��1��
��2��6.8gH2O2���״����___LCO2������ԭ������ͬ��
��.��ȥMg���е�Al�ۣ�ָ��Ӧ������Լ���д���йص����ӷ�Ӧ����ʽ��
Mg��(Al��)���Լ�___�����ӷ���ʽ____��
IV.��ƽ���·���ʽ
___NaClO��___NH3��H2O��___N2H4��___NaCl��___H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ�����Ƴ�������Ч�����������̫���ֽܷ�ˮ��ȡ��������Ҫ������ͼ��ʾ������˵����ȷ���ǣ� ��
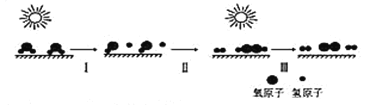
A. ������ȣ����ˮ���������ĵ������ϵ�
B. ����I����Ҫ��������
C. ���̢���м��Լ��γɣ����зǼ��Լ��γ�
D. ����Ĥ���뼼�����������������������õ�Ӧ��ǰ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯��(CaH2)�������������ˮ�������ҷ�Ӧ��ijС���������ʵ���Ʊ��⻯�ơ�����˵��������ǣ� ��
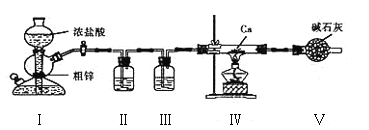
A. װ��I�������ڶ���������Ũ���ᷴӦ��ȡ����
B. װ��III��V����������ͬ
C. ֱ�����ܼ���ǰ�����Թ���ĩ���ռ����岢�鴿
D. ���������ͨ��ȡ����ˮ�����������ж��Ƿ���CaH2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��F�Ǽ�ͥ�г������л��E��ʯ�ͻ�����չˮƽ�ı�־��F��һ�ֳ����ĸ߷��Ӳ��ϡ���������ת����ϵ�ش��������⣺
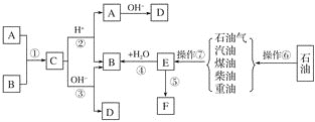
(1)�����ޡ������ߵ����Ʒֱ�Ϊ________��________��
(2)���������зе���ߵ���________��
A ���� B ú��
C ���� D ����
(3)�ڢ١���������ȡ����Ӧ����________��ԭ��������Ϊ100%�ķ�Ӧ��________��(�����)
(4)д���ṹ��ʽ��A________��F________��
(5)д����Ӧ�۵����ӷ���ʽ��___________��
(6)��Ϊ��ͥ�г���������F���������Ǵ����˼���ķ��㣬ͬʱҲ����˻�����Ⱦ��������Ⱦ��Ϊ________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com