
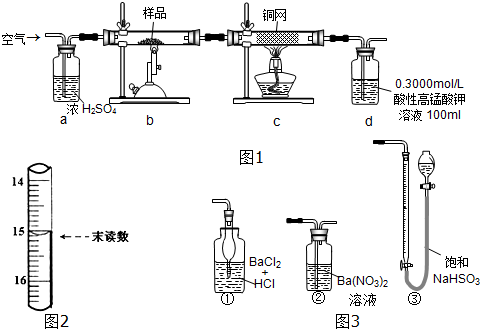
���� ��1����ȡ��ϸ����Ʒ4.000g���������ľ�ȷ�ȿ�֪������������ƽ��������
��2��װ��aΪ��ȥ�����е�ˮ��������Ӱ��ⶨ�����ͬʱ���Թ۲��������ٿ��Ʒ�Ӧ���е����ʣ�
��3������ͨ�����Ŀ���ǰ�װ���еĶ�����������ȫ���ϳ���ȫ���գ�
��4�����ᱻ���������Һ����Ϊ������̼��������ر���ԭΪ�����ӣ�
��5�����ݵζ��ܵĽṹ�����ÿ�ʼ�ͽ����������ֵ����õ����IJ�����Һ�������
��6���������շ�Ӧ�͵ζ���Ӧ�Ķ�����ϵ����������������������
��7��װ��d���������ղ��ⶨ�����ж�������ĺ��������ݶ�������Ļ�ѧ���ʽ����жϣ�
��� �⣺��1����ȡ��ϸ����Ʒ4.000g���������ľ�ȷ�ȿ�֪������������ƽ��������������ƽ�ľ�ȷ��Ϊ0.1g��
�ʴ�Ϊ�����ܣ�
��2������װ��ͼ��֪Ϊȷ�ⶨ��Ʒ��FeS2��Ʒ�Ĵ��ȣ����ÿ����е�����������������Ӧ���ɶ��������������Һ���պ��ò���ζ����㣬�����п����е�ˮ��������Ųⶨ����Ҫͨ��Ũ�����ȥ������װ�� a�������Ǹ�����ȥˮ������ͬʱ��������ð���۲��������٣�
�ʴ�Ϊ������������۲��������٣�
��3������ͨ�����Ŀ���ǰ�װ���еĶ�����������ȫ���ϳ���ȫ���գ�������
�ʴ�Ϊ���ٽ�װ���еĶ�����������ȫ�����գ�
��4�����ᱻ���������Һ����Ϊ������̼��������ر���ԭΪ�����ӣ���Ӧ�����ӷ���ʽΪ��2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��
�ʴ�Ϊ��2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��
��5�����ݵζ��ܵĽṹ�����ÿ�ʼ�ͽ����������ֵ����õ����IJ�����Һ�����Ϊ��15.10mL-0.10mL=15.00mL��
�ʴ�Ϊ��15.00��
��6�����ݷ�Ӧ�����ӷ���ʽ�������������Ӧ�ĸ���������ʵ������õ�������������ʵ��������Ԫ���غ������������������������Ϸ�Ӧ�����ӷ���ʽ����õ���2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��100mL��Һ��ʣ�����������ʵ���Ϊ��$\frac{2}{5}$��0.01500L��0.1000mol/L��10=0.006mol�����������Ӧ�ĸ���������ʵ���Ϊ��0.3000mol/L��0.1000L-0.006mol=0.024mol����Ϸ�Ӧ5SO2+2KMnO4+2H2O�TK2SO4+2MnSO4+2H2SO4�ɵã�
5FeS2��10SO2��4KMnO4
5 4
n��FeS2�� 0.024mol
n��FeS2��=0.03mol
��Ʒ��FeS2�Ĵ���Ϊ��$\frac{0.03mol��120g/mol}{4.000g}$=0.90��
�ʴ�Ϊ��0.90��
��7��ͼ3�У�ֻ�Т��ܹ����������Ӧ�������ᱵ�������������װ��d�����������ն��������п���������ˮ�������˶�������IJⶨ��
�ʴ�Ϊ���ڣ�
���� ���⿼����������ɵ�ʵ��̽��������������Ŀ�Ѷ��еȣ����ⷴӦԭ���͵ζ�ʵ��ļ����ǽ���ؼ��������ֿ���ѧ���ķ�����������������ѧʵ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������0.4 mol/L HB��Һ��0.2 mol/L NaOH��Һ�������Ϻ���Һ��pH=3��������Һ������Ũ�ȵĴ�С˳��Ϊ��c ��Na+����c ��B-����c ��H+����c ��OH-�� | |
| B�� | ����ʱ��pH��Ϊ2��CH3COOH��Һ��HCl��Һ��pH��Ϊ12�İ�ˮ��NaOH��Һ��������Һ����ˮ�����c��H+����� | |
| C�� | ������0.1 mol/L��������Һ ��NH4Al��SO4��2����NH4Cl����NH3•H2O����CH3COONH4��c ��NH$_4^+$���ɴ�С��˳���ǣ��ڣ��٣��ܣ��� | |
| D�� | 0.1 mol/L NaHB��Һ����pHΪ4��c��HB-����c��H2B����c��B$_{\;}^{2-}$�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ײ��ϡ���ָ��ֱ��Ϊ��������ʮ���IJ��ϣ������ײ����ǽ��� | |
| B�� | �ö����ЧӦ�����ֽ������Һ | |
| C�� | ��ɢ��һ����Һ�� | |
| D�� | ������FeCl3��Һ����NaOHŨ��Һ�У����Ƶ�Fe��OH��3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ӧ����������ֻ��N2 | |
| B�� | ���ⶨ��NaCN��ˮ��Һ�ʼ��ԣ�˵��CN-�ܴٽ�ˮ�ĵ��� | |
| C�� | ��������Ӧ����0.4 mol CO2������Һ�����������ӵ����ʵ���Ϊ2mol | |
| D�� | ��ȡ1 L��CN-1.02 mg/L�ķ�ˮ��������Ҫ4.0��10-5mol ����������ŷ����ŷű� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaCl | B�� | Cu | C�� | NaOH | D�� | CH3CH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
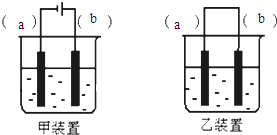 ʵ������FeSO4��Һ��NaOH��Һ��Ӧ��ȡFe��OH��2��ȴ���ѿ����ȶ��İ�ɫ��������ͬѧ�����һ���µ�ʵ�鷽����������������ɰ�ɫ��������ɫ����ת���ɺ��ɫ������������������¿հף�
ʵ������FeSO4��Һ��NaOH��Һ��Ӧ��ȡFe��OH��2��ȴ���ѿ����ȶ��İ�ɫ��������ͬѧ�����һ���µ�ʵ�鷽����������������ɰ�ɫ��������ɫ����ת���ɺ��ɫ������������������¿հף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������� | |
| B�� | ��Ŷ���C��H��N����Ԫ�ص�������Ϊ5��7��1 | |
| C�� | CO��O2����ͬѪ�쵰��ϣ��ᵼ������ȱ�� | |
| D�� | ��Ŷ��е�Ԫ�ص���������ԼΪ17.3% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� |  ������NaCl��NH4Cl�����ķ��� | |
| B�� |  ����ȥ��Fe��OH��3�����к��еĿ��������� | |
| C�� |  ��Ƥ����ƽ����ѹ��ʹҺ��˳�����µ����� | |
| D�� |  ��������Ϊ��ʽ�ζ��ܣ����ʾ����Һ�����Ϊ5.00mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4L SO3���е�ԭ����Ϊ4NA | |
| B�� | 78 g���������к��е�������Ϊ4NA | |
| C�� | ����������CO2��Ӧ����32g O2����Ӧת�Ƶĵ�����Ϊ2NA | |
| D�� | �ܱ������У���״����22.4L SO2��11.2LO2 �ڼ��ȡ��д����������³�ַ�Ӧ�������еķ�������ΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com