
| A. | 2.5×10-4m mol | B. | 5.0×10-4m mol | C. | 7.5×10-4m mol | D. | 1×10-3m mol |
分析 根据Cl元素守恒有n(KCl)=3n(AlCl3),根据Al元素守恒有n(KAlO2)=n(AlCl3),根据K元素守恒有n(K)=n(KCl)+n(KAlO2),再根据质量守恒计算加入金属钾的物质的量.
解答 解:m mL 0.25mol/L的AlCl3溶液中n(AlCl3)=0.001mL×0.25mol/L=0.00025m mol,
根据Cl元素守恒有:n(KCl)=3n(AlCl3)=3×0.00025m mol=0.00075m mol,
根据Al元素守恒有n(KAlO2)=n(AlCl3)=0.00025m mol,
所以n(K)=n(KCl)+n(KAlO2)=0.00075m mol+0.00025mmol=0.001m mol,
则加入的K的物质的量为0.001m mol=1×10-3m mol,
故选D.
点评 本题考查化学方程式的计算,题目难度中等,注意从元素守恒的角度解答较为简单,可省去书写化学方程式的中间过程,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:解答题
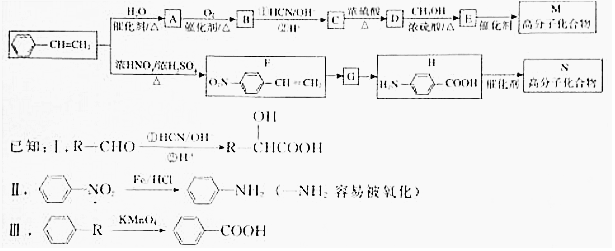
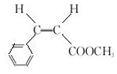 .
. 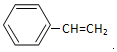 →F的反应类型为取代 反应.
→F的反应类型为取代 反应.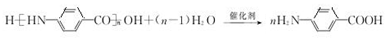 .
.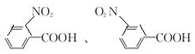 .
.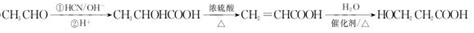 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化时要吸收大量的热,常用作制冷剂 | |
| B. | 压减燃煤、严格控车、调整产业是治理雾霾的有效措施 | |
| C. | 手机外壳上贴的碳纤维外膜是一种新型的无机非金属材料 | |
| D. | 纯碱可用于生产普通玻璃,也可用来治疗胃酸过多的病症 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
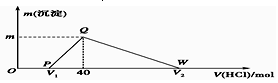
| A. | 原合金质量为0.92 g | |
| B. | 图中V2为60 | |
| C. | 整个滴定过程中Na+的浓度保持不变 | |
| D. | OP段发生的反应为:NaOH+HCl═NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ag+、PO43-、Cl- | B. | Al3+、H+、I-、HCO3- | ||
| C. | K+、Na+、NO3-、MnO4- | D. | Al3+、Mg2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2是氧化剂,S2O32-、Fe2+ 是还原剂 | |
| B. | 当有1 mol Fe3O4生成时共转移的电子为4mol | |
| C. | 若有3mol Fe2+ 参加反应,则被Fe2+还原的O2为1mol | |
| D. | 若有2mol Fe2+ 被氧化,则被Fe2+还原的O2为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-完全沉淀:2Ba2++4OH-+Al3++2SO42-═2BaBO4↓+AlO2-+2H2O | |
| C. | 向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO-3+4OH-═Mg(OH)2↓+2CO32-+2H2O | |
| D. | 向Fe(NO3)2溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
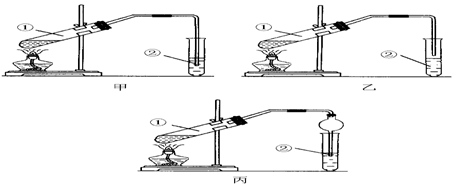
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com