
【题目】CH3COOH、H2SO3是中学化学中常见的弱酸,请回答下列问题:
(1)常温下,下列叙述能证明CH3COOH为弱酸是_________。
a. CH3COONa 溶液的pH大于7;
b.相同体积相同浓度的盐酸和醋酸溶液,分别与足量锌粉反应,放出相同体积的氢气;
c.相同体积、相同pH的盐酸和醋酸,醋酸中和NaOH的物质的量多;
d.0.01mol/L的CH3COOH溶液,PH > 2
(2)常温下,向0.1 mol·L-1 CH3COOH溶液中加蒸馏水稀释,稀释后,下列各量增大的是_________:
a.![]() b.
b.![]() c.c(OH-)
c.c(OH-)
(3)将浓度均为0.1mol/LCH3COOH和CH3COONa溶液等体积混合,测得混合液中c(CH3COO-)>c(Na+),则下列关系式中正确的是(_____)
A.c(H+) > c(OH-) B.c(H+) < c(OH-)
C.c(CH3COOH) > c(CH3COO-) D.c(CH3COOH) + c(CH3COO-)=0.1mol/L
(4)若等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液呈_______(填“酸性”,“中性”或“碱性”),原因是 _______________(用离子方程式表示)。若将pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________(填“酸性”,“中性”或“碱性”),溶液中c(Na+) ___________c(CH3COO-) (填“ >” 或“=”或“<” )。
(5)25℃时,H2SO3的电离常数Ka1=1×10-2mol/L,Ka2=6×10-3mol/L,则该温度下NaHSO3的水解平衡常数Kh=__________mol/L。
【答案】acd c AD 碱性 CH3COO- + H2O ![]() OH- + CH3COOH 酸性 < 10-12
OH- + CH3COOH 酸性 < 10-12
【解析】
(1)a.CH3COONa 溶液的pH大于7,则醋酸根离子水解使溶液呈碱性;
b.相同体积相同浓度的盐酸和醋酸溶液,分别与足量锌粉反应,放出相同体积的氢气,与酸性的强弱无关,酸物质的量相等,产生的氢气的物质的量相等;
c.相同体积、相同pH的盐酸和醋酸,醋酸中和NaOH的物质的量多;
d.0.01mol/L的CH3COOH溶液,pH > 2,说明醋酸中含有未电离的分子;
(2)a.![]() =K,K只与温度有关,温度未变,K不变;
=K,K只与温度有关,温度未变,K不变;
b.![]() =
=![]() ,加水稀释酸性减弱,c(H+)减小,K不变,其比值减小;
,加水稀释酸性减弱,c(H+)减小,K不变,其比值减小;
c. 加水稀释酸性减弱,c(H+)减小,Kw不变,则c(OH-)增大;
(3)A.根据溶液呈电中性,c(CH3COO-)+ c(OH-)=c(Na+)+c(H+);
C.由于c(H+) >c(OH-),则醋酸的电离程度大于醋酸根离子的水解程度;
D.根据物料守恒,c(CH3COOH) + c(CH3COO-)=0.1mol/L;
(4)醋酸钠为强碱弱酸盐,醋酸根离子水解,则溶液呈碱性;pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合,醋酸电离出的氢离子的物质的量与NaOH电离出的氢氧根离子的物质的量相等,但醋酸还有未电离的分子,其电离导致溶液呈酸性;
(5)根据Kh= 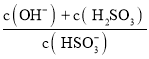 =
=![]() 计算。
计算。
(1)a.CH3COONa 溶液的pH大于7,则醋酸根离子水解使溶液呈碱性,说明醋酸为弱酸,符合题意,a正确;
b.相同体积相同浓度的盐酸和醋酸溶液,分别与足量锌粉反应,放出相同体积的氢气,与酸性的强弱无关,酸物质的量相等,产生的氢气的物质的量相等,与题意不符,b错误;
c.相同体积、相同pH的盐酸和醋酸,醋酸中和NaOH的物质的量多,说明醋酸中含有未电离的分子,醋酸为弱酸,符合题意,c正确;
d.0.01mol/L的CH3COOH溶液,pH > 2,说明醋酸中含有未电离的分子,醋酸为弱酸,符合题意,d正确;
答案为acd。
(2)a.![]() =K,K只与温度有关,温度未变,K不变,与题意不符,a错误;
=K,K只与温度有关,温度未变,K不变,与题意不符,a错误;
b.![]() =
=![]() ,加水稀释酸性减弱,c(H+)减小,K不变,其比值减小,与题意不符,b错误;
,加水稀释酸性减弱,c(H+)减小,K不变,其比值减小,与题意不符,b错误;
c. 加水稀释酸性减弱,c(H+)减小,Kw不变,则c(OH-)增大,符合题意,c正确;
答案为c。
(3)A.根据溶液呈电中性,c(CH3COO-)+ c(OH-)=c(Na+)+c(H+),已知c(CH3COO-)>c(Na+),则 c(H+)> c(OH-) ,A正确;
B.A项解析可知c(H+) >c(OH-),B错误;
C.由于c(H+) >c(OH-),则醋酸的电离程度大于醋酸根离子的水解程度,则c(CH3COOH)< c(CH3COO-),C错误;
D.根据物料守恒,c(CH3COOH) + c(CH3COO-)=0.1mol/L,D正确;
答案为AD。
(4)若等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,生成的物质醋酸钠,为强碱弱酸盐,醋酸根离子水解,则溶液呈碱性;水解的离子方程式为CH3COO- + H2O ![]() OH- + CH3COOH;pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合,醋酸电离出的氢离子的物质的量与NaOH电离出的氢氧根离子的物质的量相等,但醋酸还有未电离的分子,其电离导致溶液呈酸性;溶液中c(Na+) <c(CH3COO-);
OH- + CH3COOH;pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合,醋酸电离出的氢离子的物质的量与NaOH电离出的氢氧根离子的物质的量相等,但醋酸还有未电离的分子,其电离导致溶液呈酸性;溶液中c(Na+) <c(CH3COO-);
(5)HSO3- + H2O ![]() OH- + H2SO3,则Kh=
OH- + H2SO3,则Kh= 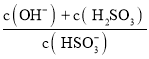 =
=![]() =10-12 mol/L。
=10-12 mol/L。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】含氮化合物在化学工业中有着重要的应用,回答下列问题:
(1)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=___________;若有1mol硝酸铵完全分解,则转移电子的数目为___________(设NA为阿伏加德罗常数的值)。
(2)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH-![]() O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
t/s | 0 | 60 | 90 | 120 | 160 | 260 | 300 | 360 | 400 |
a/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
①该反应在60~90s与90~120s内的平均反应速率分别约为___________,___________;比较两者大小可得出的结论是______________________。
②计算T℃时该反应的平衡常数为______________________。
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为______________________(写出一条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普伐他汀是一种调节血脂的药物,其结构如右图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述正确的是
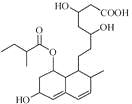
A. 能与FeCl3溶液发生显色反应
B. 能使酸性KMnO4溶液褪色
C. 1mol该物质与足量钠发生反应生成4molH2
D. 1mol该物质最多可与1molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种有机物,因其酷似奥林匹克旗中的五环(如图),科学家称其为奥林匹克烃,下列有关奥林匹克烃的说法正确的是
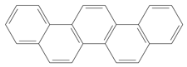
A.该烃的一氯代物只有一种
B.该烃分子中只含非极性键
C.该烃完全燃烧生成H2O的物质的量小于CO2的物质的量
D.该烃属于苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间隙法”制取,反应原理、实验装置图(加热装置都已略去)如下:![]()

已知:氯苯为无色液体,沸点132.2℃.
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是___________,冷凝管中冷水应从______(填“a”或“b”) 处通入。
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯.
①对C加热的方法是_________(填序号)
a.酒精灯加热 b.油浴加热 c.水浴加热
②D出口的气体成分有HCl、________和________;
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本.写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:_____________________;_________________;(写两个即可)
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是________________;
(5)工业生产中苯的流失情况如下:
项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
则lt苯可制得成品为________________t(只要求列式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜溶液中滴入乙二胺(H2N—CH2—CH2—NH2)即可形成配离子A,其结构如图:

(1)基态的Cu2+核外电子排布式为________。
(2)元素C、N、O的第一电离能由大到小排列顺序为_______;![]() 的空间构型为________。
的空间构型为________。
(3)A中所形成的配离子中含有的化学键类型有__________(填标号)。
a.配位键 b.极性键 c.离子键 d.非极性键
(4)乙二胺分子中氮原子轨道的杂化类型为___________,乙二胺和三甲胺 [N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是________。
(5)硫酸铜灼烧可以生成一种红色晶体,其结构如图所示,则该化合物的化学式是____。已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a=______cm。(用含ρ、NA的计算式表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热。下列有关说法错误的是( )

A. 反应后溶液中含有NO3-
B. 反应后溶液中c(H+)增大
C. 实验过程中有化合反应发生
D. 实验过程中NH3H2O的电离常数不可能发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Garnet型固态电解质被认为是锂电池最佳性能固态电解质。LiLaZrTaO材料是目前能够达到最高电导率的Garnet型电解质。某Garnet型锂电池工作原理如图所示,电池工作反应原理为:C6Lix+Li1xLaZrTaO=LiLaZrTaO+C6。下列说法不正确的是( )
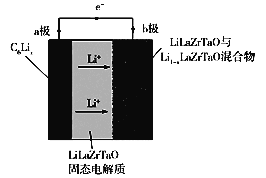
A.b极为正极,a极发生氧化反应
B.LiLaZrTaO固态电解质起到传导Li+的作用
C.b极反应为:xLi++Li1xLaZrTaOxe=LiLaZrTaO
D.当电池工作时,每转移x mol电子,b极增重7x g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛化合物常见价态有+2和+4。钛白粉(TiO2,两性氧化物)用途广泛。工业上由高钛渣(主要成分为Ti3O5,还含有TiO2、Fe2O3等)制取钛白粉的主要工艺过程如下:
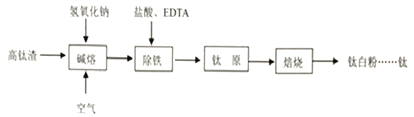
(1)写出碱熔步骤所发生反应的化学方程式____________、____________。
(2)实验测定EDTA加入量(EDTA和Fe3+的物质的量之比)对 Ti4+和Fe3+溶出率的影响如图所示。由图可知,EDTA的加入量为____________时除铁效率最佳,理由是____________。

(3)在实验室模拟除铁净化后的实验步骤:①向钛原料中加入稀硫酸生成偏钛酸(H2TiO3)沉淀,反应结束后过滤;②洗涤;③……;④在650℃下高温焙烧得到较纯的钛白粉固体。步骤③的实验目的是____________,需要用到的试剂有____________。
(4)测定钛白粉纯度:称取试样0.200g在CO2气氛下用金属铝将钛(IV)还原成钛(Ⅲ),还原后的溶液以NH4SCN为指示剂,用0.08mol/L的 NH4Fe(SO4)2标准液滴定,滴定终点时消耗标准液29.20mL,钛白粉的纯度为____________。(保留三位有效数字)
(5)最新研究发现也可以用图示装置由TiO2获得金属钛。装置中阳极的电极反应方程式为____________,在制备金属钛前后,整套装置中CaO的总量____________(填写“增大”、“减小”或者“不变”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com