
元素 | a | b | c | d | e | f | g |
最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
用化学符号完成下列问题:
(1)元素b与L层上有6个电子的元素结合成稳定化合物,其化学式为____________。
(2)最高价氧化物对应水化物酸性最强的是____________,碱性最强的是____________。
(3)所形成的气态氢化物最稳定的是____________。
(4)元素c的最高价氧化物对应水化物又称____________性氢氧化物,它与元素g的氢化物水溶液反应的化学方程式为__________________________;它与元素a的最高价氧化物对应水化物的溶液反应可表示为_________________________。
(5)a—g元素中,最高价氧化物对应水化物呈酸性,且酸性由弱到强的顺序依次是_________________________________________________。
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
| A | D | |||
| E | G | M |

查看答案和解析>>
科目:高中化学 来源: 题型:
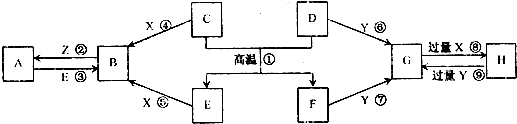
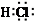
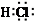
| ||
| ||
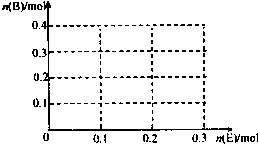
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com