
����Ŀ��ij���㾭A���л��ϳ��зdz���Ҫ��ԭ�ϣ�ͨ���������������ʺɱ�Ϊ118����˴Ź�����������5���壬�����֮��Ϊ1��2��2��2��3���䱽����ֻ��һ��ȡ��������������AΪԭ�Ϻϳɸ߷��ӻ�����F��I��·��ͼ���Իش��������⣺
��1��A�Ľṹ��ʽΪ
��2��E�еĹ�����������
��3��G�Ľṹ��ʽΪ
��4����Ӧ�ڡ��ܵķ�Ӧ���ͷֱ���
��5����Ӧ�ޡ������ɵĸ߷��ӻ�����ķ�Ӧԭ���Ƿ���ͬ�������ͬ������ͬ����
��6��д�����з�Ӧ�Ļ�ѧ����ʽ����Ӧ������Ӧ��
��7����������������C��ͬ���칹�����֣������������칹��a��������������ȡ����
b�������ϵ�һ�ȴ���������
c���������Ȼ�����Һ��ɫ
d����1mol�������м��������Ľ����ƿɲ���1mol�⣮
���𰸡�
��1��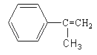
��2���ǻ����Ȼ�
��3��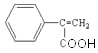
��4��ȡ����Ӧ����ȥ��Ӧ
��5������ͬ
��6��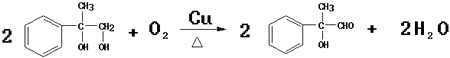 ��n
��n 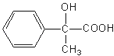
![]()
 +��n��1��H2O
+��n��1��H2O
��7��5
���������⣺����CԪ�ء�HԪ���غ�ȷ�������ķ���ʽΪC6H12 �� �ڴ�����������H2�����ӳɷ�Ӧ������2��2���������飬������Ľṹ��ʽΪ��CH3��3C��CH=CH2������1mol��2mol HCl��ȫ�ӳɣ������������2��˫����1��������1mol�ȴ����ܺ�4mol����������ȫȡ����Ӧ�����ȴ����������4��Hԭ�ӣ�����ԭ����������2��Hԭ�ӣ��ݴ�ȷ������ͨ��������÷�����A����Է�������Ϊ118���䱽����ֻ��һ��ȡ��������˴Ź�����������5���壬�����֮��Ϊ1��2��2��2��3����A����ֻ��Ϊ��  ���������A��������Ȼ�̼��Һ�ɷ����ӳɷ�Ӧ�õ�±����B��±�������������Ƶ�ˮ��Һ�з���ȡ����Ӧ�������ʣ�C
���������A��������Ȼ�̼��Һ�ɷ����ӳɷ�Ӧ�õ�±����B��±�������������Ƶ�ˮ��Һ�з���ȡ����Ӧ�������ʣ�C  ������ͭ����������������Ӧ���ɶ�Ӧ��ȩ�����ʣ�D
������ͭ����������������Ӧ���ɶ�Ӧ��ȩ�����ʣ�D 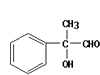 ��ȩ��������ͭ���������������£����������ɶ�Ӧ���E
��ȩ��������ͭ���������������£����������ɶ�Ӧ���E 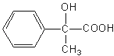 ����E������Ũ���������£�
����E������Ũ���������£� 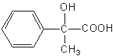 ����ȥ�ǻ����������ʣ�G
����ȥ�ǻ����������ʣ�G 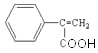 ������G��Ũ����������£�����״�����������Ӧ�������ʣ�H 2��������ϩ�����������H�ɷ����Ӿ۷�Ӧ��������I��
������G��Ũ����������£�����״�����������Ӧ�������ʣ�H 2��������ϩ�����������H�ɷ����Ӿ۷�Ӧ��������I��  ��������E
��������E 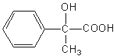 �����Ȼ��ɺ��ǻ����������۷�Ӧ����F
�����Ȼ��ɺ��ǻ����������۷�Ӧ����F 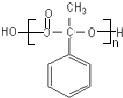 ����1���������Ϸ�����֪��A�Ľṹ��ʽΪ��
����1���������Ϸ�����֪��A�Ľṹ��ʽΪ��  ���ʴ�Ϊ��
���ʴ�Ϊ��  ����2���������Ϸ�����֪��E�Ľṹ��ʽΪ
����2���������Ϸ�����֪��E�Ľṹ��ʽΪ  �����л�������к��еĹ�����Ϊ�ǻ����Ȼ����ʴ�Ϊ���ǻ����Ȼ�����3�����ݷ�����֪��G�Ľṹ��ʽΪ��
�����л�������к��еĹ�����Ϊ�ǻ����Ȼ����ʴ�Ϊ���ǻ����Ȼ�����3�����ݷ�����֪��G�Ľṹ��ʽΪ�� 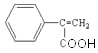 ���ʴ�Ϊ��
���ʴ�Ϊ�� 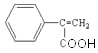 ����4�����ݷ�����֪����Ӧ��Ϊ±�������������Ƶ�ˮ��Һ�з���ȡ����Ӧ��������C����Ӧ��ΪE������Ũ���������£�
����4�����ݷ�����֪����Ӧ��Ϊ±�������������Ƶ�ˮ��Һ�з���ȡ����Ӧ��������C����Ӧ��ΪE������Ũ���������£� 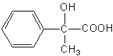 ��ȥ�ǻ�������ȥ��Ӧ��������G���ʴ�Ϊ��ȡ����Ӧ����ȥ��Ӧ����5���������Ϸ�������Ӧ��H��Ϊ����̼̼˫������Ϊ�Ӿ����ɸ߷���I����Ϊ������E
��ȥ�ǻ�������ȥ��Ӧ��������G���ʴ�Ϊ��ȡ����Ӧ����ȥ��Ӧ����5���������Ϸ�������Ӧ��H��Ϊ����̼̼˫������Ϊ�Ӿ����ɸ߷���I����Ϊ������E 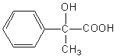 ��Ϊ���Ȼ��ɺ��ǻ������Է������۷�Ӧ���ɸ߷���F���������ɵĸ߷��ӻ�����ķ�Ӧԭ���Dz���ͬ���ʴ�Ϊ������ͬ����6����Ӧ��Ϊ
��Ϊ���Ȼ��ɺ��ǻ������Է������۷�Ӧ���ɸ߷���F���������ɵĸ߷��ӻ�����ķ�Ӧԭ���Dz���ͬ���ʴ�Ϊ������ͬ����6����Ӧ��Ϊ 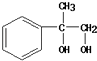 ����������
���������� 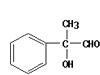 ����Ӧ�Ļ�ѧ����ʽΪ��
����Ӧ�Ļ�ѧ����ʽΪ�� 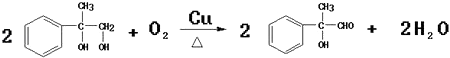 �� ��Ӧ��Ϊ
�� ��Ӧ��Ϊ 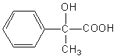 ��һ��������ת���ɸ߷���F
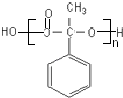
��һ��������ת���ɸ߷���F  ����Ӧ�Ļ�ѧ����ʽΪ��n
����Ӧ�Ļ�ѧ����ʽΪ��n 
![]()
 +��n��1��H2O��
+��n��1��H2O��
�ʴ�Ϊ�� 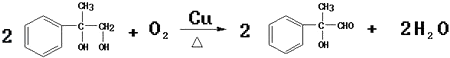 ��n
��n 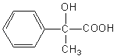
![]()
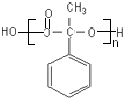 +��n��1��H2O����7��CΪ
+��n��1��H2O����7��CΪ 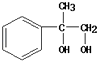 ��ͬ���칹��a��������������ȡ������b�������ϵ�һ�ȴ��������֣���Ϊ��λ�ṹ��c���������Ȼ�����Һ��ɫ��˵������һ��ȡ����Ϊ���ǻ���d����1mol�������м��������Ľ����ƿɲ���1mol������˵����һ��������һ���ǻ��������������ȡ��������Ϊ��OH�ͩ�CH2CH2CH2OH�����ߩ�OH�ͩ�CH2CHOHCH3 �� ���ߩ�OH�ͩ�CHOHCH2CH3 �� ���ߩ�OH�ͩ�CH��CH3��CH2OH�����ߩ�OH�ͩ�COH��CH3��2 �� ��5�֣��ʴ�Ϊ��5��
��ͬ���칹��a��������������ȡ������b�������ϵ�һ�ȴ��������֣���Ϊ��λ�ṹ��c���������Ȼ�����Һ��ɫ��˵������һ��ȡ����Ϊ���ǻ���d����1mol�������м��������Ľ����ƿɲ���1mol������˵����һ��������һ���ǻ��������������ȡ��������Ϊ��OH�ͩ�CH2CH2CH2OH�����ߩ�OH�ͩ�CH2CHOHCH3 �� ���ߩ�OH�ͩ�CHOHCH2CH3 �� ���ߩ�OH�ͩ�CH��CH3��CH2OH�����ߩ�OH�ͩ�COH��CH3��2 �� ��5�֣��ʴ�Ϊ��5��
����CԪ�ء�HԪ���غ�ȷ�������ķ���ʽΪC6H12 �� �ڴ�����������H2�����ӳɷ�Ӧ������2��2���������飬������Ľṹ��ʽΪ��CH3��3C��CH=CH2������1mol��2mol HCl��ȫ�ӳɣ������������2��˫����1��������1mol�ȴ����ܺ�4mol����������ȫȡ����Ӧ�����ȴ����������4��Hԭ�ӣ�����ԭ����������2��Hԭ�ӣ��ݴ�ȷ������ͨ��������÷�����A����Է�������Ϊ118���䱽����ֻ��һ��ȡ��������˴Ź�����������5���壬�����֮��Ϊ1��2��2��2��3����A����ֻ��Ϊ��  ���������A��������Ȼ�̼��Һ�ɷ����ӳɷ�Ӧ�õ�±����B��±�������������Ƶ�ˮ��Һ�з���ȡ����Ӧ�������ʣ�C
���������A��������Ȼ�̼��Һ�ɷ����ӳɷ�Ӧ�õ�±����B��±�������������Ƶ�ˮ��Һ�з���ȡ����Ӧ�������ʣ�C 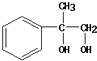 ������ͭ����������������Ӧ���ɶ�Ӧ��ȩ�����ʣ�D
������ͭ����������������Ӧ���ɶ�Ӧ��ȩ�����ʣ�D 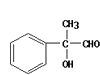 ��ȩ��������ͭ���������������£����������ɶ�Ӧ���E
��ȩ��������ͭ���������������£����������ɶ�Ӧ���E 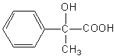 ����E������Ũ���������£�
����E������Ũ���������£� 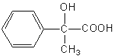 ����ȥ�ǻ����������ʣ�G
����ȥ�ǻ����������ʣ�G 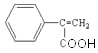 ������G��Ũ����������£�����״�����������Ӧ�������ʣ�H 2��������ϩ�����������H�ɷ����Ӿ۷�Ӧ��������I��
������G��Ũ����������£�����״�����������Ӧ�������ʣ�H 2��������ϩ�����������H�ɷ����Ӿ۷�Ӧ��������I��  ��������E
��������E  �����Ȼ��ɺ��ǻ����������۷�Ӧ����F
�����Ȼ��ɺ��ǻ����������۷�Ӧ����F 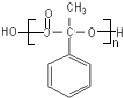 ���ݴ˽��н��
���ݴ˽��н��


 ״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����Ҫ��NaCl��������500mL 0.2molL��1NaCl��Һ���ش��������⣺
��1��Ӧ����������ƽ��ȡNaCl����g�����ƣ�23 �ȣ�35.5��
��2����ͼ���ʾ10mL��Ͳ��Һ���λ�ã�A��B��B��C�̶ȼ����1mL������̶�AΪ8����Ͳ��Һ��������mL��
��3����ʵ������ͼ����ʾ�������������������������Һ��Ũ���к�Ӱ�죿���ƫ�ߡ�����ƫ�͡�����Ӱ�족��A������ʱ��ˮ�����̶�����
B�����ն���ʱ���ӹ۲�Һ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ͬ����������ǣ� ��
A. H2��D2B. ���Ͱ���C. O2��O3D. ���ʯ��C60
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ�س�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦʽΪ��
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
������������ȷ����
A. �ŵ�ʱ�����ķ�ӦΪ��Zn-2e-+2OH-![]() Zn(OH)2
Zn(OH)2
B. ���ʱ������ӦΪ��Fe(OH)3-3e-+5OH-![]() FeO42-+4H2O
FeO42-+4H2O
C. �ŵ�ʱÿת��3 mol���ӣ�������1 mol K2FeO4����ԭ
D. �ŵ�ʱ����������Һ�ļ��Լ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ȡ����Ȳ�����г���������H2S��CO2��ˮ������Ϊ�˵õ����﴿������Ȳ���壬ѡ�������ʵ�鷽���У� ��
A.ͨ��NaOH��ͨ��ŨH2SO4 �� ��ͨ��ʯ��ˮ
B.ͨ��CuSO4��Һ����ͨ��ʯ��ˮ
C.ͨ���������ף���ͨ����ˮCaCl2
D.ͨ�������ļ�ʯ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1L���ݵ��ܱ������У�����֤�����淴ӦN2+3H2![]() 2NH3�Ѵﵽƽ��״̬����
2NH3�Ѵﵽƽ��״̬����
A. c��N2����c��H2����c��NH3��=1��3��2
B. һ��N��N ���ѵ�ͬʱ����3��H-H����
C. ������������ʱ�����������ܶȲ��ٸı�
D. v����N2���T2 v�棨NH3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ����Ҫ500mL��0.1mol/L��NaOH��Һ����ͨ�����²������ƣ�
��1���ٰѳ����õ�g����NaOH����С�ձ��У�����������ˮ�ܽ⣮Ϊ�ӿ��ܽ����ʹ�������������ƣ����裻�ڰѢ�������Һ��ȴ�����º�С��ת�������������ƺ��
�ۼ���������ˮ��Һ�����̶���12cm�������������������ƣ�С�ĵμ�����ˮ����Һ��Һ����͵���̶������У�
������������ˮϴ�Ӳ��������ձ�23�Σ�ÿ��ϴ�ӵ���Һ��С��ת������ƿ��������ҡ�ȣ�
�ݽ�����ƿ���������ҡ�ȣ�
��2������������ȷ��˳����������ţ���
��3����������Һ���ܶ�Ϊ1.06g/mL�������Һ����������Ϊ ��
��4����ȡ��20mL��õ�NaOH��Һ��������ˮϡ�ͳ�c��Na+��=0.01mol/L����Һ����ϡ�ͺ���Һ�����ΪmL��
��5��������500mL��0.1mol/L��NaOH��Һʱ�����в����е��ᵼ�½��ƫ�ͣ����������д����������ֽ����NaOH�ڽ��ձ��е���Һת�Ƶ�����ƿʱ������������ƿ��
�۶���ʱ���ӿ̶��ߢܶ���ʱ���ӿ̶���
�ݸɾ�������ƿδ�����������������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2S��Һ�и������ӵ����ʵ���Ũ�ȹ�ϵ����ȷ����( )
A. c(Na+)��c(S2-)��c(OH-)��c(HS-) B. c(Na+)+c(H+)��c(HS-)+2c(S2-)+c(OH-)
C. c(Na+)��2c(HS-)+2c(S2-)+2c(H2S) D. c(OH-)��c(H+) + c(HS-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�˿������ǧ�����ʷ���Ļ����Ŵ�Ⱦ������ij�֡������������˿�á����������Ҫ�ɷ���һ���Σ��ܴٽ���˿�����˿����������ˮ�����ȥ��ʹ˿����ɫ��ס��ʸ�������ɫ����������֡�����������ǣ� ��
A.ʳ��
B.���
C.��ľ��
D.����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com