
【题目】甲、乙均为1L的恒容密闭容器,向甲中充入1molCH4和1molCO2,乙中充入1molCH4和nmolCO2,在催化剂存在下发生反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
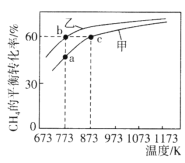
A.该反应的正反应是吸热反应
B.773K时,该反应的平衡常数小于12.96
C.H2的体积分数:![]()
D.873K时,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2mol,平衡不发生移动
【答案】AB
【解析】
A.温度升高,CH4的平衡转化率增大,说明温度升高有利于反应正向进行,则正反应为吸热反应,故A正确;
B.873K时,c点CH4的平衡转化率为60%,列“三段式”:

则K(c)=![]() =12.96,温度升高,CH4的平衡转化率增大,平衡正向移动,平衡常数增大,则773K时该反应的平衡常数小于12.96,故B正确;
=12.96,温度升高,CH4的平衡转化率增大,平衡正向移动,平衡常数增大,则773K时该反应的平衡常数小于12.96,故B正确;
C.根据图像,相同温度下乙中甲烷的平衡转化率大于甲中,则n>1,b、c点甲烷的平衡转化率相等,则两点平衡时体系中CH4、CO、H2物质的量分别相等,但b中CO2物质的量大于c中,则H2的体积分数:![]() ,故C错误;
,故C错误;
D.873K时,甲容器中甲烷的转化率为60%,列三段式:
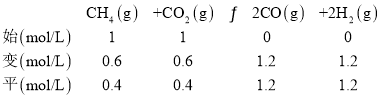
平衡常数K=![]() =12.96,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2mol,Qc=
=12.96,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2mol,Qc=![]() =51.84>K=12.96,平衡逆向移动,故D错误;
=51.84>K=12.96,平衡逆向移动,故D错误;
答案选AB。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】键线式是表达有机化合物结构的一种方式,如H2N—CH2—CH2—OH 用键线式可以表达为 ![]() 。吡喹酮(H)是一种治疗血吸虫病的药物,合成路线如下图所示:
。吡喹酮(H)是一种治疗血吸虫病的药物,合成路线如下图所示:
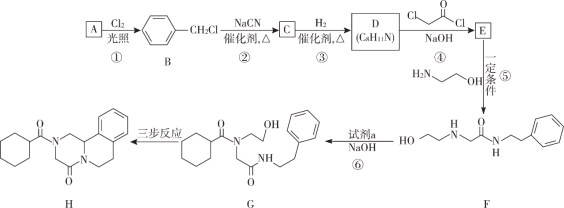
已知:I R-Cl+NaCN![]() R-CN+NaCl
R-CN+NaCl
ii 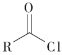 +R′—NH—R"+NaOH
+R′—NH—R"+NaOH![]()
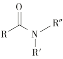 +NaCl+H2O(R、R′表示烃基,R"表示羟基或H)
+NaCl+H2O(R、R′表示烃基,R"表示羟基或H)
(1)A 属于芳香烃,其名称是____________ 。
(2)②的反应类型是_____________ 。
(3)B 的一种同分异构体,含苯环且核磁共振氢谱中出现三组峰,其结构简式为_____________ 。
(4)③中 1 mol C 理论上需要消耗 ___________mol H2 生成 D。
(5)④的化学方程式是_____________ 。
(6) 试剂 a 的结构简式是 ____________________。
(7) G→H 分为三步反应,J 中含有 3 个六元环,写出 I、J 的结构简式________________、__________________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯在多种条件下发生水解反应:CH3COOC2H5 + H2OCH3COOH+C2H5OH。已知该反应的速率随c(H+)的增大而加快。下图为CH3COOC2H5的水解速率随时间的变化图。下列说法错误的是( )
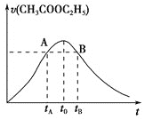
A.反应初期水解速率增大可能是溶液中c(H+)逐渐增大所致
B.A、B两点表示的c(CH3COOC2H5)相等
C.图中t0时反应达到平衡状态
D.CH3COOC2H5的转化率tA时低于tB时
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg与Br2反应可生成具有强吸水性的MgBr2,该反应剧烈且放出大量的热。实验室采用如图装置制备无水MgBr2。下列说法错误的是
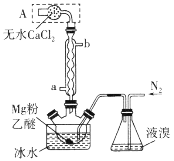
A.a为冷却水进水口
B.装置A的作用是吸收水蒸气和挥发出的溴蒸气
C.实验时需缓慢通入N2,防止反应过于剧烈
D.不能用干燥空气代替N2,因为副产物MgO会阻碍反应的进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL![]() 的HR溶液中逐滴滴入
的HR溶液中逐滴滴入![]() 的
的![]() 溶液,所得溶液pH及导电能力变化如图
溶液,所得溶液pH及导电能力变化如图![]() 下列分析不正确的是
下列分析不正确的是![]()
![]()

A. ![]() 点导电能力增强,说明HR为弱酸
点导电能力增强,说明HR为弱酸
B. b点溶液![]() ,此时酸碱恰好中和
,此时酸碱恰好中和
C. c点溶液存在![]() 、
、![]()
D. b、c两点水的电离程度:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 乳酸薄荷醇酯(![]() )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B. 乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C. 用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3
D. 分子式为C9H12的苯的同系物,若苯环上只有一个取代基,则其一溴代物最多有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在钯基催化剂表面上,甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用*标注。

(1)![]() 的△H=_____________kJ·mol-1;该历程中最大能垒(活化能)E正=____________kJ·mol-1,写出该步骤的化学方程式_________________。
的△H=_____________kJ·mol-1;该历程中最大能垒(活化能)E正=____________kJ·mol-1,写出该步骤的化学方程式_________________。
(2)在一定温度下,CO和H2混合气体发生反应:![]() ,反应速率υ=υ正-υ逆=k正c(CO)·c2(H2)-k逆c(CH3OH),k正、k逆分别为正、逆反应速率常数。达到平衡后,若加入高效催化剂,
,反应速率υ=υ正-υ逆=k正c(CO)·c2(H2)-k逆c(CH3OH),k正、k逆分别为正、逆反应速率常数。达到平衡后,若加入高效催化剂,![]() 将___________(填“增大”、“减小”或“不变”);若升高温度,
将___________(填“增大”、“减小”或“不变”);若升高温度,![]() 将____________(填“增大”、“减小”或“不变”)。
将____________(填“增大”、“减小”或“不变”)。
(3)353K时,在刚性容器中充入CH3OH(g),发生反应:![]() 。体系的总压强p随时间t的变化如表所示:
。体系的总压强p随时间t的变化如表所示:
t/min | 0 | 5 | 10 | 15 | 20 | ∞ |
p/kPa | 101.2 | 107.4 | 112.6 | 116.4 | 118.6 | 121.2 |
①若升高反应温度至373K,则CH3OH(g)分解后体系压强p∞(373K)___________121.2kPa(填“大于”、“等于”或“小于”),原因是________________________。
②353K时,该反应的平衡常数KP=__________(kPa)2(KP为以分压表示的平衡常数,计算结果保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质N2、H2O、Na2O2、CaCl2、KOH、NaF中,既含有离了键,又含有共价键的物质是_____,属于共价化合物的是__________。
(2)用电子式表示CaCl2的形成过程:________________。
(3)氮化钠(Na3N)是科学家制备的一种重要化合物,它与水作用产生NH3。请写出NH3的电子式是____________。
(4)Na3N与盐酸反应生成两种盐,反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:FeF3溶液接近无色。某同学据此进行以下实验,依据上述实验无法获得的结论是

A.FeF3是弱电解质
B.④中发生的离子反应为FeF3+3SCN-Fe(SCN)3+3F-
C.相同条件下,结合Fe3+的能力:SCN->F->OH-
D.向Fe(SCN)3溶液中加入NaF固体,溶液颜色会变浅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com