
| A. | 高压钠灯发出的黄光射程远.透雾能力强,常用于道路和广场的照明 | |
| B. | 镁合金密度小,硬度和强度大,可用于制造火箭、导弹和飞机的部件 | |
| C. | 水玻璃常用于浸泡有特殊用途的木材、纺织品等达到耐腐蚀和防火的目的 | |
| D. | 氢氧化铁胶体具有吸附性,能吸附水中的悬浮颗粒并沉降,可用作消毒剂 |
分析 A.钠的焰色反应为黄色;
B.镁合金的强度高、机械性能好,其成分镁是制造汽车、飞机、火箭的重要材料,享有“国防金属”的美誉;
C.水玻璃为硅酸钠水溶液具有防腐作用和阻燃作用;
D.氢氧化铁不能用于杀菌消毒.
解答 解:A.钠的焰色反应为黄色,穿透力强,可用于广场照明,高压钠灯常用于道路和广场的照明,故A正确;
B.镁合金的强度高、机械性能好,可用于制造火箭和飞机的部件,故B正确;
C.水玻璃为硅酸钠水溶液具有防腐作用和阻燃作用,人们经常把具有特殊用途的木材、纺织品等用水玻璃浸泡,这样加工的产品既耐腐蚀又不易着火,故C正确;
D.氢氧化铁不能用于杀菌消毒,不能作用消毒剂,故D错误.
故选D.
点评 本题综合考查元素化合物知识,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | |
| B. | 标准状况下,22.4LNO和11.2L氧气混合,气体的分子总数为1.5 NA | |
| C. | 7.8 g Na2O2含有的阴离子数目为0.1 NA | |
| D. | 80mL10mol/L的浓盐酸与足量MnO2反应,转移电子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
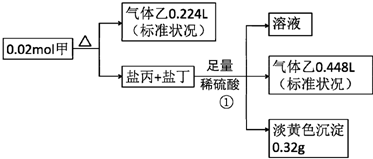
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
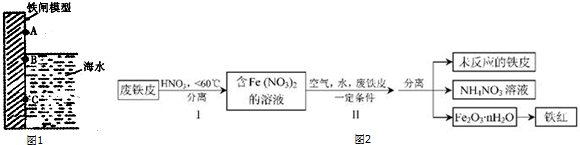
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径 (×10-10m) | 0.37 | 1.86 | 1.43 | 0.99 | 0.75 | 0.74 | |
主要化合价 | 最高 正价 | +1 | +1 | +3 | +7 | +5 | - |
| 最低 负价 | -1 | - | - | -1 | -3 | -2 | |
| A. | H2Q的还原性和稳定性大于RH3 | |
| B. | Y、Z、M三种元素的最高价氧化物的水化物两两之间会反应 | |
| C. | 化合物XM,YM都是电解质,熔融状态下都能电解 | |
| D. | 元素Z、M组成的化合物熔化时破坏了离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
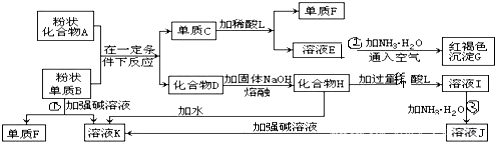
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
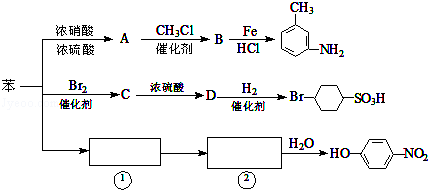
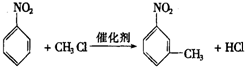 .
.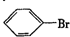 ,②
,②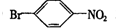 .
.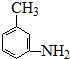 的所有原子不是(填“是”或“不是”)在同一平面上.
的所有原子不是(填“是”或“不是”)在同一平面上.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 手上滴了浓硫酸立即用大量水冲洗 | |
| B. | 皮肤上沾了苯酚马上用浓氢氧化钠溶液洗涤 | |
| C. | 金属钠着火,迅速用沙土灭火 | |
| D. | 水银温度计不慎打破,迅速将水银收集水封,收集不起来的用硫粉盖上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com