
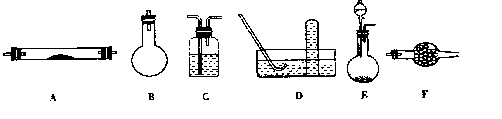
| A£®N2ŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ·“Ӧɜ³ÉNH3 |
| B£®NH3¾“ß»ÆŃõ»ÆÉś³ÉNO |
| C£®NOÓėO2·“Ӧɜ³ÉNO2 |
| D£®ÓÉNH3ÖĘĢ¼ļ§»ņĮņļ§ |
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®0.12 mol | B£®0.11 mol | C£®0.09 mol | D£®0.08 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
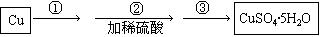
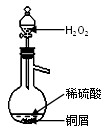
| A£®Al2(SO4)3 | B£®Na2CO3 | C£®KNO3 | D£®FeSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
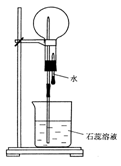
 £¬Ē”ŗĆŹ¹ĘųĢåĶźČ«ČÜÓŚĖ®”£ŌņĶØČė
£¬Ē”ŗĆŹ¹ĘųĢåĶźČ«ČÜÓŚĖ®”£ŌņĶØČė µÄĢå»żĪŖ¶ąÉŁ£æ(3·Ö)
µÄĢå»żĪŖ¶ąÉŁ£æ(3·Ö)²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
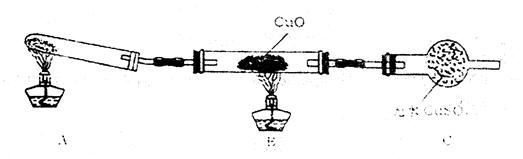
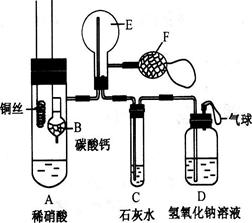
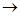 Cu+ Cu2+ £©”£ĒėÄćÉč¼ĘŅ»øö¼ņµ„µÄŹµŃé¼ģŃéøĆŗģÉ«ĪļÖŹÖŠŹĒ·ńŗ¬ÓŠCu2O ”£
Cu+ Cu2+ £©”£ĒėÄćÉč¼ĘŅ»øö¼ņµ„µÄŹµŃé¼ģŃéøĆŗģÉ«ĪļÖŹÖŠŹĒ·ńŗ¬ÓŠCu2O ”£²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com