
ĖįŠŌĢõ¼žĻĀ£¬ĪżŌŚĖ®ČÜŅŗÖŠÓŠSn2+”¢Sn4+Į½ÖÖÖ÷ŅŖ“ęŌŚŠĪŹ½”£SnSO4ŹĒŅ»ÖÖÖŲŅŖµÄĮņĖįŃĪ£¬¹ć·ŗÓ¦ÓĆÓŚ¶ĘĪż¹¤Ņµ£¬ĘäÖʱøĀ·ĻßČēĻĀ£ŗ
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©SnCl2ÓĆŃĪĖį¶ų²»ÓĆĖ®Ö±½ÓČܽāµÄŌŅņŹĒ
¼ÓČėĪż·ŪµÄ×÷ÓĆŹĒ
£Ø2£©·“Ó¦IÉś³ÉµÄ³ĮµķĪŖSnO£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
£Ø3£©¼ģŃé³ĮµķŅŃ¾”°Ļ“µÓ”±øɾ»µÄ²Ł×÷ŹĒ£ŗ £Ø3·Ö£©
£Ø4£©·“Ó¦¢ņĮņĖįµÄ×÷ÓĆÖ®Ņ»ŹĒæŲÖĘČÜŅŗµÄpH”£ČōČÜŅŗÖŠc(Sn2+)=1.0mol”¤L”Ŗ1£¬ŌņŹŅĪĀĻĀÓ¦æŲÖĘČÜŅŗpH ”££ØŅŃÖŖ£ŗKsp[Sn(OH)2]=1.0”Į10”Ŗ26£©
£Ø5£©ĖįŠŌĢõ¼žĻĀ£¬SnSO4»¹æÉÓĆ×÷Ė«ŃõĖ®µÄČ„³ż¼Į£¬ŹŌŠ“³öĖł·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
ӣ
£Ø6£©³±ŹŖ»·¾³ÖŠ£¬¶ĘĪżĶ¼“Ź¹Īż²ćĘĘĖšŅ²ÄÜ·ĄÖ¹ŠĪ³ÉĶĀĢ£¬Ēė½įŗĻÓŠ¹ŲµÄŌĄķ½āŹĶĘäŌŅņ£ŗ
ӣ
£Ø1£©ŅÖÖĘSn2+Ė®½ā£¬ ·ĄÖ¹Sn2+±»Ńõ»Æ £Ø2£©SnCl2 + Na2CO3 =" SnO" + CO2”ü+2NaCl£Ø3£©Č”ÉŁĮæ×īŗóŅ»“ĪĻ“µÓŅŗÓŚŹŌ¹ÜÖŠ£¬µĪČė¼øµĪAgNO3ČÜŅŗ£¬ČōĪŽ°×É«³ĮµķÉś³É£¬ŌņĖµĆ÷³ĮµķŅŃĻ“µÓøɾ»£Ø3·Ö£©£Ø4£©Š”ÓŚ1 £Ø2·Ö”£ČōŠ“³É”Ü1øų1·Ö£© £Ø5£©Sn2+ + H2O2 + 2H+ = Sn4+ + 2H2O £Ø6£©³±ŹŖ»·¾³ÖŠ£¬SnÓėCu¹¹³ÉŌµē³Ų£¬Sn×÷ĪŖøŗ¼«£¬±£»¤Õż¼«Cu²»±»Ńõ»Æ
½āĪöŹŌĢā·ÖĪö£ŗ£Ø1£©SnCl2Ņ×Ė®½āÉś³É¼īŹ½ĀČ»ÆŃĒĪż£¬“ęŌŚĘ½ŗāSn Cl2+H2O?Sn£ØOH£©Cl+HCl£¬¼ÓČėŃĪĖį£¬Ź¹øĆĘ½ŗāĻņ×óŅĘ¶Æ£¬ŅÖÖĘSn2+Ė®½ā£»Sn2+Ņ×±»Ńõ»Æ£¬¼ÓČėSn·Ū³żµ÷½ŚČÜŅŗpHĶā£¬»¹·ĄÖ¹Sn2+±»Ńõ»Æ£»£Ø2£©·“Ó¦¢ńµĆµ½³ĮµķŹĒSnO£¬SnŌŖĖŲ»ÆŗĻ¼ŪĪŖ±ä»Æ£¬ŹōÓŚ·ĒŃõ»Æ»¹Ō·“Ó¦£¬Ķ¬Ź±Éś³ÉĘųĢ壬øĆĘųĢåĪŖ¶žŃõ»ÆĢ¼£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗSn2++CO32-ØTSnO”ż+CO2”ü£»£Ø3£©¼ģŃé³ĮµķŅŃ¾”°ĘÆĻ“”±øɾ»µÄ·½·ØŹĒ£ŗČ”×īŗóŅ»“ĪĻ“µÓŅŗ£¬ĻņĘäÖŠ¼ÓČėAgNO3ČÜŅŗ£¬ČōĪŽ³Įµķ£¬ŌņĖµĆ÷Ļ“µÓøɾ»£»£Ø4£©øł¾Ż Ksp[Sn£ØOH£©2]=1.0”Į10-26=c£ØOH-£©2”Įc£ØSn2+£©£¬½«c£ØSn2+£©=1.0mol?L-1“ųČĖæɵĆc£ØOH-£©=10-13mol/L£¬c£ØH+£©=0.1mol/L£¬¹ŹPHŠ”ÓŚ1£¬Sn2+ĶźČ«³Įµķ£»£Ø5£©ĖįŠŌĢõ¼žĻĀ£¬SnSO4»¹æÉŅŌÓĆ×÷Ė«ŃõĖ®Č„³ż¼Į£¬Ė«ŃõĖ®ÓŠĒæŃõ»ÆŠŌ£¬½«Sn2+Ņ×±»Ńõ»ÆĪŖSn4+£¬×ŌÉķ±»»¹ŌĪŖĖ®£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗSn2++H2O2+2H+ØTSn4++2H2O£»£Ø6£©³±ŹŖ»·¾³ÖŠ£¬SnÓėCu¹¹³ÉŌµē³Ų£¬Sn×÷ĪŖøŗ¼«£¬±£»¤Õż¼«Cu²»±»Ńõ»Æ”£
æ¼µć£ŗĪļÖŹ·ÖĄėŗĶĢį“æµÄ·½·ØŗĶ»ł±¾²Ł×÷×ŪŗĻÓ¦ÓĆ£»ÖʱøŹµŃé·½°øµÄÉč¼Ę”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ij¶žŌŖĖį(»ÆѧŹ½ÓĆH2B±ķŹ¾)ŌŚĖ®ÖŠµÄµēĄė·½³ĢŹ½ŹĒH2B===H£«£«HB££»HB£ H£«£«B2£”£»Ų“šĻĀĮŠĪŹĢā”£
H£«£«B2£”£»Ų“šĻĀĮŠĪŹĢā”£
(1)Na2BČÜŅŗĻŌ_____(Ģī”°ĖįŠŌ”±”¢”°ÖŠŠŌ”±»ņ”°¼īŠŌ”±)£¬ĄķÓÉŹĒ_______(ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾)”£
(2)ŌŚ0.1 mol”¤L£1µÄNa2BČÜŅŗÖŠ£¬ĻĀĮŠĮ£×ÓÅØ¶Č¹ŲĻµŹ½ÕżČ·µÄŹĒ____”£
A£®c(B2£)£«c(HB£)£«c(H2B)£½0.1 mol”¤L£1
B£®c(Na£«)£«c(OH£)£½c(H£«)£«c(HB£)
C£®c(Na£«)£«c(H£«)£½c(OH£)£«c(HB£)£«2c(B2£)
D£®c(Na£«)£½2c(B2£)£«2c(HB£)
(3)ŅŃÖŖ0.1 mol”¤L£1 NaHBČÜŅŗµÄpH£½2£¬Ōņ0.1 mol”¤L£1 H2BČÜŅŗÖŠµÄĒāĄė×ÓµÄĪļÖŹµÄĮæÅضČæÉÄÜ____0.11 mol”¤L£1(Ģī”°<”±”¢”°>”±»ņ”°£½”±)£¬ĄķÓÉŹĒ_____”£
(4)0.1 mol”¤L£1 NaHBČÜŅŗÖŠø÷ÖÖĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ĻĀ±ķŹĒ¼øÖÖČõµē½āÖŹµÄµēĄėĘ½ŗā³£Źż”¢ÄŃČܵē½āÖŹµÄČܶȻżKsp£Ø25”ę£©”£
| µē½āÖŹ | µēĄė·½³ĢŹ½ | µēĄė³£ŹżK | Ksp |
| H2CO3 | H2CO3 HCO3££«H£« HCO3££«H£«HCO3£  CO32££«H£« CO32££«H£« | K1£½4.31”Į10£7 K2£½5.61”Į10£11 | £ |
| C6H5OH | C6H5OH C6H5O££«H£« C6H5O££«H£« | 1.1”Į10£10 | £ |
| H3PO4 | H3PO4 H2PO4££«H£« H2PO4££«H£«H2PO4£  HPO42££«H£« HPO42££«H£«HPO42£  PO43££«H£« PO43££«H£« | K1£½7.52”Į10£3 K2£½6.23”Į10£6 K1£½2.20”Į10£13 | £ |
| NH3”¤H2O | NH3”¤H2O OH££«NH4£« OH££«NH4£« | 1.76”Į10£5 | £ |
| BaSO4 | BaSO4£Øs£© Ba2£«£«SO42£ Ba2£«£«SO42£ | £ | 1.07”Į10£10 |
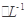 C6H5OHČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č
C6H5OHČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č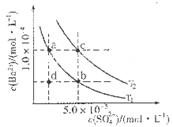
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŅŃÖŖijČÜŅŗÖŠÖ»“ęŌŚOH£”¢H+”¢NH4+”¢Cl£ĖÄÖÖĄė×Ó£¬Ä³Ķ¬Ń§ĶĘ²āĘäĄė×ÓÅØ¶Č“óŠ”Ė³ŠņÓŠČēĻĀĖÄÖÖ¹ŲĻµ£ŗ
| A£®c(NH4+)£¾c(Cl£)£¾c(OH£)£¾c(H+) | B£®c(Cl£)£¾c(H+)£¾c(NH4+)£¾c(OH£) |
| C£®c(Cl£)£¾c(NH4+)£¾c(H+)£¾c(OH£) | D£®c(NH4+)£¾c(OH£)£¾c(Cl£)£¾c(H+) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
¹¤ŅµÉĻĻņ°±»ÆµÄCaSO4Šü×ĒŅŗÖŠĶØČėŹŹĮæCO2£¬æÉÖĘČ”(NH4)2SO4£¬ĘäĮ÷³ĢČēĻĀĶ¼ĖłŹ¾£¬ŅŃÖŖCaSO4µÄKsp£½9.1”Į10£6£¬CaCO3µÄKsp£½2.8”Į10-9£¬Ēė»Ų“š£ŗ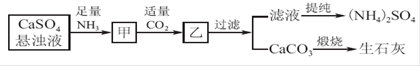
£Ø1£©Ļņ¼×ÖŠĶØČė¹żĮæCO2_____£ØĢī”°ÓŠ”±»ņ”°²»”±£©ĄūÓŚCaCO3ŗĶ(NH4)2SO4µÄÉś³É£¬ŌŅņŹĒ_______________________________________________________________”£
£Ø2£©Ö±½ÓÕōøÉĀĖŅŗµĆµ½µÄ(NH4)2SO4Ö÷ŅŖŗ¬ÓŠµÄŌÓÖŹŹĒ________(Ģīŗ¬Įæ×ī¶ąµÄŅ»ÖÖ)”£
£Ø3£©¹ųĀÆĖ®¹øÖŠŗ¬ÓŠµÄCaSO4£¬æÉĻČÓĆNa2CO3ČÜŅŗ½žÅŻ£¬Ź¹Ö®×Ŗ»ÆĪŖŹčĖÉ£¬Ņ×ČÜÓŚĖįµÄCaCO3£¬¶ųŗóÓĆĖį³żČ„”£
¢ŁCaSO4×Ŗ»ÆĪŖCaCO3µÄĄė×Ó·½³ĢŹ½ĪŖ____________________________________”£
¢ŚĒė·ÖĪöCaSO4×Ŗ»ÆĪŖCaCO3µÄŌĄķ£ŗ__________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
³£ĪĀĻĀĖ®“ęŌŚµēĄėĘ½ŗā£¬H2O H++OH? £¬Ēė»Ų“š£ŗ
H++OH? £¬Ēė»Ų“š£ŗ
¢ŁČōÉżøßĪĀ¶Č£¬µēĄė³Ģ¶Č½« £¬ČÜŅŗ³Ź ŠŌ”£
¢ŚĻņĘäÖŠ¼ÓČėÉŁĮæĻ”°±Ė®£¬Ė®µÄµēĄėĘ½ŗā ŅĘ¶Æ£¬ČÜŅŗµÄPH ”£
¢ŪČōĻņĘäÖŠ¼ÓČėÉŁĮæNaHSO4ČÜŅŗ£¬Ė®µÄĄė×Ó»ż³£Źż £¬ÓÉĖ®µēĄė³öµÄc(H+) c(OH_)£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
°“ŅŖĒóĶź³ÉĻĀĮŠ»Æѧ·“Ó¦Ź½
£Ø1£©ĮņĖįĒāÄĘŌŚĖ®ČÜŅŗÖŠµÄµēĄė·½³ĢŹ½”””””” ””””””””””””””””£»
£Ø2£©Na2CO3ČÜŅŗĖ®½āµÄĄė×Ó·½³ĢŹ½”””””””””””””””””””””””””” ””£»
£Ø3£©Al2(SO4)3ČÜŅŗÓėNaHCO3ČÜŅŗ»ģŗĻ·“Ó¦µÄĄė×Ó·½³ĢŹ½”””””” ””””””£»
£Ø4£©Mg3N2ÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½”””””””” ””””””””””””””””””””””£»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
µēĄė¶Č±ķŹ¾µē½āÖŹµÄĻą¶ŌĒæČõ£¬µēĄė¶ČµÄ¶ØŅå£ŗ
¦Į£½£ØŅѵēĄėµÄµē½āÖŹ·Ö×ÓŹż£ÆČÜŅŗÖŠŌÓŠµē½āÖŹµÄ×Ü·Ö×ÓŹż£©”Į100%”£
ŅŃÖŖ25”ꏱ¼øÖÖĪļÖŹ(Ī¢Į£)µÄµēĄė¶Č(ČÜŅŗÅØ¶Č¾łĪŖ0.1 mol”¤L£1)ČēĻĀ±ķ£ŗ
| ±ąŗÅ | ĪļÖŹ(Ī¢Į£) | µēĄė¶Č¦Į |
| A | ĮņĖįČÜŅŗ(µŚŅ»²½ĶźČ«µēĄė)£ŗ µŚ¶ž²½ HSO4- H£«£«SO42- H£«£«SO42- | 10% |
| B | ĮņĖįĒāÄĘČÜŅŗ£ŗ HSO4- H£«£«SO42 H£«£«SO42 | 29% |
| C | “×Ėį£ŗ CH3COOH CH3COO££«H£« CH3COO££«H£« | 1.33% |
| D | ŃĪĖį£ŗ HCl£½H£«£«Cl£ | 100% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŃĒĮ×Ėį£ØH3PO3£©ŹĒ¶žŌŖĖį£¬H3PO3ČÜŅŗ“ęŌŚµēĄėĘ½ŗā£ŗH3PO3 H+ + H2PO3£”£ŃĒĮ×ĖįÓė×ćĮæNaOHČÜŅŗ·“Ó¦£¬ÉśŗĶNa2HPO3”£
H+ + H2PO3£”£ŃĒĮ×ĖįÓė×ćĮæNaOHČÜŅŗ·“Ó¦£¬ÉśŗĶNa2HPO3”£
£Ø1£©¢ŁŠ“³öŃĒĮ×ĖįÓėÉŁĮæNaOHČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½_____________________________________”£
¢ŚÄ³ĪĀ¶ČĻĀ£¬0.1000 mol”¤L£1µÄH3PO3ČÜŅŗpHµÄ¶ĮŹżĪŖ1.6£¬¼““ĖŹ±ČÜŅŗÖŠc (H+) = 2.5”Į10£2 mol”¤L£1£¬³żOH”ŖÖ®ĶāĘäĖūĄė×ÓµÄÅضČÓÉŠ”µ½“óµÄĖ³ŠņŹĒ £¬øĆĪĀ¶ČĻĀH3PO3µēĄėĘ½ŗāµÄĘ½ŗā³£ŹżK= ”££ØH3PO3µŚ¶ž²½µēĄėŗöĀŌ²»¼Ę£¬½į¹ū±£ĮōĮ½Ī»ÓŠŠ§Źż×Ö£©
¢ŪĻņH3PO3ČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗÖĮÖŠŠŌ£¬ĖłµĆČÜŅŗÖŠc£ØNa+£©_______ c£ØH2PO3-£©+ 2c£ØHPO32-£©£ØĢī”°>”±”¢ ”°<”± »ņ”°=”±£©”£
£Ø2£©ŃĒĮ×Ėį¾ßÓŠĒ滹ŌŠŌ£¬æÉŹ¹µāĖ®ĶŹÉ«£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½_______________________”£
£Ø3£©µē½āNa2HPO3ČÜŅŗŅ²æɵƵ½ŃĒĮ×Ėį£¬×°ÖĆŹ¾ŅāĶ¼ČēĻĀ£ŗ
ĖµĆ÷£ŗŃōĤֻŌŹŠķŃōĄė×ÓĶعż£¬ŅõĤֻŌŹŠķŅõĄė×ÓĶعż”£
¢ŁŅõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ_____________________________”£
¢Ś²śĘ·ŹŅÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com