
分析 乙烯为平面结构,故丙烯分子中至少有6个原子位于同一平面,由于单键可以旋转,故甲基上的1个氢原子也可能在这个平面内,故丙烯分子中最多有7个原子位于同一平面.
解答 解:乙烯为平面结构,故丙烯分子中至少有6个原子位于同一平面,由于单键可以旋转,故甲基上的1个氢原子也可能在这个平面内,故丙烯分子中最多有7个原子位于同一平面,丙烯与HBr发生加成反应可以得到两种产物,结构简式分别为:CH3-CHBr-CH3 ,CH3-CH2-CH2Br,故答案为:7;CH3-CHBr-CH3 ,CH3-CH2-CH2Br.
点评 本题以乙烯为模型,考查丙烯的结构,难度中等.侧重学生知识迁移能力的培养.


 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:解答题
 O3氧化海水中I-是大气中碘的主要来源.将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,发生反应如下:
O3氧化海水中I-是大气中碘的主要来源.将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,发生反应如下: .
.| 实验编号 | 实验目的 | 反应物 | 温度 | 反应前溶液的pH |
| A | 对照组 | O3+NaI+H2SO4 | 25℃ | 5.2 |
| B | 研究FeCl2对I3-生成速率的影响 | O3+NaI+H2SO4+FeCl2 | 25℃ | 5.2 |
| C | 研究温度对I3-生成速率的影响 | O3+NaI+H2SO4 | 5℃ | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 事实 | 现象或解释 |
| A | 不法分子燃烧硫磺熏制银耳 | 二氧化硫有还原性 |
| B | 可用浓氨水检验输送煤气的管道是否有泄漏 | 出现白烟处是煤气泄漏点 |
| C | 泡沫灭火器使用的物质是硫酸铝和碳酸钠 | 二者混合发生双水解反应生成二氧化碳和氢氧化铝 |
| D | 医院里常用来紫外线灯进行杀菌消毒 | 紫外线能使蛋白质变性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液化、汽化、风化、熔化等都属于物理变化 | |
| B. | 液化石油气、汽油、花生油主要成分都是碳氢化合物 | |
| C. | 水分子之间可以形成氢键,所以水比硫化氢稳定 | |
| D. | 提出原子在一定轨道上运动的原子结构模型是波尔 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
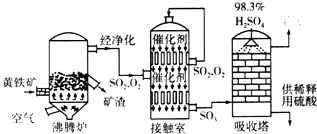
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
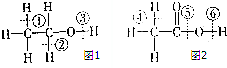 (1)乙醇分子的结构式可表示如图1,在乙醇和钠反应时,③(填序号,下同)键断裂,在Cu催化和加热条件下与O2反应时,①②键断裂.
(1)乙醇分子的结构式可表示如图1,在乙醇和钠反应时,③(填序号,下同)键断裂,在Cu催化和加热条件下与O2反应时,①②键断裂.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜电极上发生氧化反应 | |
| B. | 电池工作一段时间后,甲池的c(SO42-)减小 | |
| C. | 电池工作一段时间后,乙池溶液的总质量增加 | |
| D. | 阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com