
��һ���������ܱ������м���2mol A��0.6mol C��һ������B�������塣һ�������·�����Ӧ��������Ũ����ʱ��仯��ͼһ��ʾ��ͼ��Ϊt2ʱ�̺�ı䷴Ӧ������ƽ����ϵ�з�Ӧ������ʱ��仯����������ĸ��ζ����ı�һ�ֲ�ͬ����������֪t3��t??4��Ϊʹ�ô�����ͼһ��t0��t1��c��B��δ������
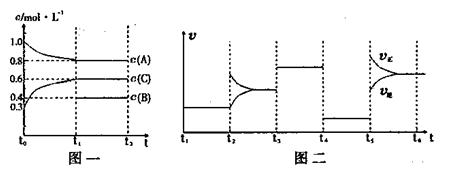
����˵������ȷ���ǣ� ��
A�����¶��¸÷�Ӧ�Ļ�ѧ����ʽ2A��g��+B��g��![]() 2C��g��
2C��g��
B��t4��t5�θı������Ϊ��Сѹǿ
C��B����ʼ���ʵ���Ϊ1.0mol
D������ͬ�����£�����ʼʱ�����м���a mol A��bmol B��cmol C��Ҫ�ﵽt1ʱ��ͬ����ƽ�⣬a��b��cҪ���������Ϊa+![]() ��2.4 �� b+
��2.4 �� b+![]() ��1.2
��1.2

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 6 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ٵƾ���ʹ�������������ܻ������ŵ㣮һ���¶��£��ڵ��ٵƵ����ڷ���������������ڵ��ݱ��ϵ��ٿ��Է������µĿ��淴Ӧ��
���ٵƾ���ʹ�������������ܻ������ŵ㣮һ���¶��£��ڵ��ٵƵ����ڷ���������������ڵ��ݱ��ϵ��ٿ��Է������µĿ��淴Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��10�֣����ٵƾ���ʹ�������������ܻ������ŵ㡣һ���¶��£��ڵ��ٵƵ����ڷ���������������ڵ��ݱ��ϵ��ٿ��Է������µĿ��淴Ӧ��
W��s��+ I2��g�� WI2��g����H<0
Ϊģ��������Ӧ����450��ʱ��һ���Ϊ2L�ĺ����ܱ������м���0.1mol�ⵥ�ʺ��������٣�2min��Ӧ�ﵽƽ�⣬��õ�����Ũ��Ϊ0.005 mol��L-1����ش��������⣺
��1��ǰ�������ڵ������ķ�Ӧ����Ϊ �� ��
��2���ܹ�˵��������Ӧ�Ѿ��ﵽƽ��״̬���� �� ��
A��I2��WI2��Ũ�����
B������������ѹǿ���ٱ仯
C��W���������ٱ仯
D����λʱ���ڣ����������ĵ����ʵ�����⻯�����ɵ����ʵ������
E�������ڻ��������ܶȱ��ֲ���
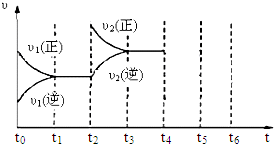
��3����ͼΪ�÷�Ӧ��450��ʱ��ʱ�䡪����ͼ����t2ʱ�̸ı��������������� �� ����t4ʱ�̽�����ѹ����һ�루������״̬���䣩�����ָ�������t6������ͼ�л���t4��t6ʱ����ڴ�������ͼ��������Ӧ�����ϱ��Ϧ�3(��)����3(��)
t0 t1 t2 t3 t4 t5 t6 t
��4�������˿�¶�Ϊ660�棬���ݱ��¶�Ϊ350�档����ݻ�ѧ��Ӧԭ�������ڵ����ڳ�����ܹ��ӳ���˿������ԭ�� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ�����и�����һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�˹��̵���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̡�
I.���һЩ��ѧ���о����ø����ӵ����Ե�SCY�մɣ��ܴ���H+��ʵ�鵪�Ĺ̶�һ��ⷨ�ϳɰ����������˵�����������ת���ʡ��ܷ�ӦʽΪ��N2(g)��3H2(g)  2NH3(g)�����ڵ�ⷨ�ϳɰ��Ĺ����У�Ӧ��H2���ϵ�ͨ��_________����������������� ������һ�缫ͨ��N2���õ缫�ķ�ӦʽΪ__________________________��
2NH3(g)�����ڵ�ⷨ�ϳɰ��Ĺ����У�Ӧ��H2���ϵ�ͨ��_________����������������� ������һ�缫ͨ��N2���õ缫�ķ�ӦʽΪ__________________________��
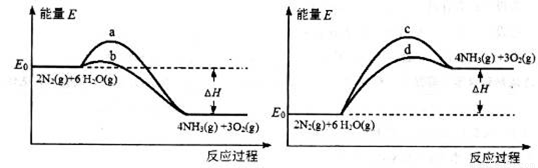
II.�ݱ�������һ�������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ����Ҫ����ΪNH3����Ӧ�ķ�Ӧ����ʽΪ��2N2(g)��6H2O(g)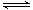 4NH3(g)��3O2(g) ��H��Q��
4NH3(g)��3O2(g) ��H��Q��
��1��������Ӧ��ƽ�ⳣ������ʽΪ_______________��
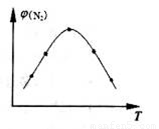
��2��ȡ��ݵ����N2��H2O�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3�����ֱ���������ͬ�ĺ����ܱ������У����¶Ȳ���ͬ������·�����Ӧ����Ӧ��ͬʱ���õ������������ �뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ����������Ӧ��Q________0�����������������=������
�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ����������Ӧ��Q________0�����������������=������
��3����������Ӧ���д���������·���������ͼ��ʾ��a��b��c��d���������У��ܱ�ʾ��Ӧ��ϵ�����仯����_______��ѡ����ĸ���ţ���ͼ�С�H�ľ���ֵΪ1530kJ��mol-1��
III.Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2(g)��3H2(g) 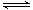 2NH3(g) ��H����93.0kJ/mol��
2NH3(g) ��H����93.0kJ/mol��
�ش��������⣺
��1�����II�е����ݣ���O2(g)��2H2(g)��2H2O(g)�ġ�H��______________��
��2����һ���¶��£���1molN2��3mol H2����������������ܱ������з�����Ӧ���ﵽƽ��״̬ʱ��������������ʵ���Ϊ2.8mol��
�ٴ�ƽ��ʱ��H2��ת���ʦ�1��______________��
������ͬ�����£�����ʼʱֻ��NH3���ڸ������У��ﵽƽ��״̬ʱNH3��ת����Ϊ��2������1����2��1ʱ������ʼʱNH3�����ʵ���n(NH3)��_____________mol��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com