
£Ø1£©·“Ó¦Ē°ŗóµÄŃ¹ĒæÖ®±Č”£
£Ø2£©Ę½ŗāŹ±»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮ攣
 ¾«Ó¢æŚĖćæØĻµĮŠ“š°ø
¾«Ó¢æŚĖćæØĻµĮŠ“š°ø Ó¦ÓĆĢāµć²¦ĻµĮŠ“š°ø
Ó¦ÓĆĢāµć²¦ĻµĮŠ“š°ø דŌŖ¼°µŚĻµĮŠ“š°ø
דŌŖ¼°µŚĻµĮŠ“š°ø Ķ¬²½°ĀŹżĻµĮŠ“š°ø
Ķ¬²½°ĀŹżĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
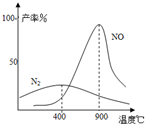 £Ø2009?֊ɽģÄā£©¹¤ŅµŗĻ³É°±ÓėÖʱøĻõĖįŅ»°ćæÉĮ¬ŠųÉś²ś£¬Į÷³ĢČēĻĀ£ŗ
£Ø2009?֊ɽģÄā£©¹¤ŅµŗĻ³É°±ÓėÖʱøĻõĖįŅ»°ćæÉĮ¬ŠųÉś²ś£¬Į÷³ĢČēĻĀ£ŗ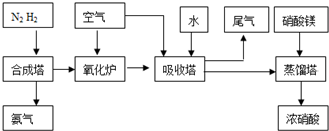
| Ź±¼ä£Øh£©ÅØ¶Č£Ømol/L£© | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0 | 0.200 | 0.600 | C3 | C3 |
| 1 |
| a |
| 1 |
| a |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| 1 |
| 2 |
| Ź±¼ä/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c£ØNH3£©/£Ømol?L-1£© | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
 “ĖĢõ¼žĻĀ£¬øĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāŹ±£¬µŖĘųµÄÅضČĪŖ
“ĖĢõ¼žĻĀ£¬øĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāŹ±£¬µŖĘųµÄÅضČĪŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
°ŃĒāĘųŗĶµŖĘųŅŌ1”Ć1µÄĪļÖŹµÄĮæÖ®±Č·ÅČėŅ»ČŻ»ż¹Ģ¶ØµÄČŻĘ÷ÖŠ£¬²āµĆĘ½ŗāŹ±µŖĘųµÄ×Ŗ»ÆĀŹĪŖ20%Ź±£¬Ēó£ŗ
£Ø1£©·“Ó¦Ē°ŗóµÄŃ¹ĒæÖ®±Č”£
£Ø2£©Ę½ŗāŹ±»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮ攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2009Äź¹ć¶«Ź”֊ɽŹŠøßæ¼»ÆŃ§Ä£ÄāŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
| Ź±¼ä£Øh£©ÅØ¶Č£Ømol/L£© | 1 | 2 | 3 | 4 | |
| N2 | 1.500 | 1.400 | 1.200 | C1 | C1 |
| H2 | 4.500 | 4.200 | 3.600 | C2 | C2 |
| NH3 | 0.200 | 0.600 | C3 | C3 |
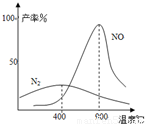
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com