
【题目】现有a mol/L 的NaX和b mol/L的NaY两种盐溶液。下列说法正确的是
A.若a=b且c(X-)= c(Y-)+ c(HY),则HX为强酸
B.若a=b且pH(NaX)>pH(NaY),则c(X-)+ c(OH-)> c(Y-)+ c(OH-)
C.若a>b且c(X-)= c(Y-),则酸性HX>HY
D.若两溶液等体积混合,则c(Na+)=(a+b) mol/L(忽略混合过程中的体积变化)
【答案】A
【解析】
试题分析:A.若a=b,且c(X-)=c(Y-)+c(HY),说明HX完全电离,所以能说明HX为强酸,故A 正确;B.若a=b且pH(NaX)>pH(NaY),根据电荷守恒得c(Na+)+c(H+)=c(X-)+c(OH-),c(Na+)+c(H+)=c(Y-)+c(OH-),根据物料守恒得两种溶液中c(Na+)相等,根据溶液的PH知,X-的水解程度大于Y-,所以NaX中氢离子浓度小于NaY,所以c(X-)+c(OH-)<c(Y-)+c(OH-),故B错误;C.若a>b且c(X-)=c(Y-),说明X- 的水解程度大于Y-,酸根离子水解程度越大,其相应酸的酸性越弱,则酸性HX<HY,故C错误;D.若两溶液等体积混合,钠离子不水解,但溶液体积增大一倍,所以则c(Na+)=![]() mol/L,故D错误;故选A。
mol/L,故D错误;故选A。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是重要的溶剂和替代燃料,工业常以CO和H2的混合气体为原料一定条件下制备甲醇。
(1)甲醇与乙醇互为 ;完全燃烧时,甲醇与同物质的量的汽油(设平均组成为C8H18)消耗O2量之比为 。
(2)工业上常用“水煤气法”获得CO和H2,其反应原理如下:
C(s) + H2O(g) ![]() CO(g) + H2(g) CO(g) + H2O(g)
CO(g) + H2(g) CO(g) + H2O(g) ![]() CO2(g) + H2(g)
CO2(g) + H2(g)
某水煤气样品中含0.2LCO、0.5LCO2,则该样品中含H2 L。
(3)工业上还可以通过下列途径获得H2,其中节能效果最好的是 。
A. 高温分解水制取H2:2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
B. 电解水制取H2:2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
C. 甲烷与水反应制取H2:CH4 + H2O![]() 3H2 + CO
3H2 + CO
D. 在光催化剂作用下,利用太阳能分解水制取H2:2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
(4)在2L的密闭容器中充入1molCO和2molH2,一定条件下发生反应:CO(g)+2H2(g) ![]() CH3OH(g) 测得CO和CH3OH(g)浓度变化如图所示。
CH3OH(g) 测得CO和CH3OH(g)浓度变化如图所示。

① 从反应开始到平衡,氢气的平均反应速率v(H2)= mol·(L·min)—1。
② 能够判断该反应达到平衡的是 (填选项)。
A.CO、H2和CH3OH三种物质的浓度相等
B.密闭容器中混合气体的密度不再改变
C.CH3OH分解的速率和CH3OH生成的速率相等
D.相同时间内消耗1 mol CO,同时消耗1 mol CH3OH
(5)为使合成甲醇原料的原子利用率达100%,实际生产中制备水煤气时还使用CH4,则生产投料时,n(C)∶n(H2O)∶n(CH4)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为4种常见溶液中溶质的质量分数和物质的量浓度:
溶 质 | HCl | NaOH | CH3COOH | HNO3 |
溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
物质的量浓度/mol·L-1 | 11.8 | 14.3 | 10.6 | 13.8 |
这4种溶液中密度最小的是( )
A.HCl B.NaOH C.CH3COOH D.HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中存在XO3―,且X为短周期元素,则一定能在该溶液中大量共存的离子组是( )
A.Na+、H+、SO42-、I-
B.Na+、Ca2+、CO32-、Al3+
C.Na+、K+、Fe2+、H+
D.K+、SO42-、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、下列物质的转化或分离方法的序号填在横线上(每一项只填写一种方法,用序号填空)。①溶解 ②裂解 ③分馏 ④裂化 ⑤干馏 ⑥蒸馏 ⑦过滤 ⑧电解 ⑨萃取
(1)将海水淡化 。
(2)从海水得到的无水MgC12中提取金属镁 。
Ⅱ、下图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。
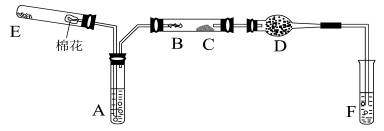
图中:A为无水乙醇(沸点为78℃),
B为绕成螺旋状的细铜丝或银丝,
C为无水CuSO粉末,
D为碱石灰,
F为新制的氢氧化铜悬浊液。
已知: 含—CHO的物质在加热条件下与新制的Cu(OH)2悬浊液反应生成砖红色沉淀.
(1)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号) 。
(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是_____________。
D处使用碱石灰的作是 。
(3) E处是一种纯净物,其反应方程式为 。
(4)写出乙醇发生催化氧化的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1molL-1HCl溶液滴定10.0mL浓度为0.1molL-1Na2CO3溶液,所得滴定曲线如图所示。下列微粒浓度大小关系正确的是
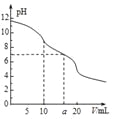
A. 当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
B. 当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-)
C. 当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D. 当V=a时:c(Na+)=c(Cl-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。
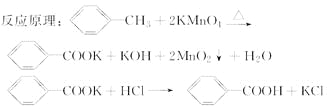
实验方法:一定量的甲苯和KMnO4溶液在100 ℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
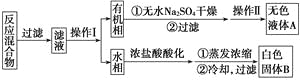
已知:苯甲酸分子量122,熔点122.4 ℃,在25 ℃和95 ℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为________,操作Ⅱ为________。
(2)无色液体A是________,定性检验A的试剂是________,现象是________。
(3)测定白色固体B的熔点,发现其在115 ℃开始熔化,达到130 ℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在完成表中内容。
序号 | 实验方案 | 实验现象 | 结果 |
① | 将白色固体B加入水中,加热溶解,________ | 得到白色晶体和无色滤液 | |
② | 取少量滤液于试管中,________ | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________ | ________ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220 g产品,配成100 mL苯甲酸溶液,移取25.00 mL溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,产品中苯甲酸质量分数的计算结果为________(保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关实验室制乙烯的说法中,不正确的是
A.温度计的水银球要伸入到反应物的液面以下
B.反应过程中溶液的颜色逐渐变黑
C.生成的乙烯气体中混有少量有刺激性气味的气体
D.加热时不要太急,使温度缓慢上升至170℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com