
【题目】[化学——选修3:物质结构与性质]
X、Y、Z、Q、R、T是前四周期原子序数依次增大的六种元素,其中X元素形成的气体单质密度最小,Y元素氢化物的水溶液呈碱性,Z、R元素最外层电子数相同且Z的原子序数为R的一半,Q的原子半径在第三周期中最大,T是目前应用最广泛的金属。回答下列问题:
(1)T在周期表中的位置是 ,其M层上的电子排布式为 。
(2)Y、Z、R的第一电离能由大到小的顺序为 (用元素符号表示)。
(3)根据等电子体原理,Y2Z分子的结构式为 。
(4)YZ能被TRZ4溶液吸收生成配合物[T(YZ)(X2Z)5]RZ4,该配合物中含有的化学键类型有 ,RZ42-离子中R原子的杂化方式为 。
(5)由Q与Z、R可形成多种化合物,写出Q2Z2的电子式: ,Q2Z熔点比Q2R高,其原因是 。
(6)QX晶体的结构与NaCl相同,则X-的配位数为 ,若Q+与最邻近X-的核间距离为a pm,阿伏加德罗常数为NA,则QX晶体的密度为 g/cm3。
【答案】
(1)第四周期第Ⅷ族(1分) 3s23p63d6(1分)
(2)N>O>S(2分)
(3)N=N=O(2分)
(4)离子键、共价键、配位键(2分) sp3(杂化) (1分)
(5)![]() (1分)
(1分)
Na2O中O2-半径比Na2S中S2-半径小,所以Na2O晶格能更大,则熔点更高(2分)
(6)6(1分) ![]() ×1030(2分)
×1030(2分)
【解析】
试题分析:前四周期的元素中X元素形成的气体单质密度最小,说明X为氢元素;Y元素氢化物的水溶液呈碱性,说明Y为氮元素;X、Y、Z、Q、R、T的原子序数依次增大,且Z、R元素最外层电子数相同且Z的原子序数为R的一半,说明Z为氧元素、R为硫元素;Q的原子半径在第三周期中最大,说明Q为钠元素;T是目前应用最广泛的金属,说明T为铁元素。
(1)铁在周期表中的位置是第四周期第Ⅷ族,其M层上的电子排布式为3s23p63d6。
(2)N、O、S的第一电离能由大到小的顺序为N>O>S。
(3)N2O分子与CO2互为等电子体,根据等电子体原理,N2O也为直线型,其结构式为N=N=O。
(4)NO、H2O分子内有共价键,Fe2+与NO、H2O有配位键,[Fe(NO)(H2O)5]2+与SO42-有离子键,所以配合物[Fe(NO)(H2O)5]SO4中含有的化学键类型有离子键、共价键、配位键;SO42-中S原子的杂化方式为sp3(杂化) 。
(5)Na2O2的电子式为![]() ;Na2O中O2-半径比Na2S中S2-半径小,所以Na2O晶格能更大,则熔点更高。。
;Na2O中O2-半径比Na2S中S2-半径小,所以Na2O晶格能更大,则熔点更高。。
(6)NaH晶体的结构与NaCl相同,则H-的配位数为6;Na+与最邻近H-的核间距离为a pm,则晶胞的边长为2a×10-10 cm,晶胞中含有4个NaH,所以晶体的密度=晶胞质量÷晶胞体积=(![]() ×4)÷(2a×10-10 cm)3=
×4)÷(2a×10-10 cm)3=![]() ×1030 g/cm3。
×1030 g/cm3。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下表为元素周期表中短周期的一部分,其中Y元素的核电荷数为M与N元素核电荷数之和。下列说法正确的是

A.氢化物稳定性:N>Z,因为N的氢化物中存在氢键
B.简单离子半径:N>X,是因为它们具有相同的电子层结构且X的核
电荷数更大
C.元素的非金属性:M>Y,是因为M单质能与YN2反应生成Y单质
D.熔沸点:YN2>MN2,是因为YN2的分子间作用力强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应A2(g)+B2(g)![]() 2AB(g),达到反应限度的标志是( )
2AB(g),达到反应限度的标志是( )
A. 容器内气体的总压强不随时间的变化而变化
B. 单位时间内有nmolA2生成,同时就有nmolB2生成
C. 单位时间内有nmolA2生成,同时就有2nmolAB生成
D. 单位时间内有nmolB2发生反应,同时就有2nmolAB生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修5有机化学基础]
阿司匹林是一种历史悠久的解热镇痛药,对预防血栓和脑梗有很好的作用,M是一种防晒剂,它们的结构简式分别为:![]() 和
和![]() 。由A出发合成路线如下:
。由A出发合成路线如下:

已知:Ⅰ.
Ⅱ.![]()
根据以上信息回答下列问题
(1)M中含氧官能团的名称 。
(2)写出 H→I过程中的反应类型 。F的结构简式 。
(3)写出D → E转化过程中①的化学方程式 。
(4)由H→I的过程中可能出现多种副产物,其中一种分子式为C16H12O2Cl2,写出该副产物的结构简式 。
(5)阿司匹林有多种同分异构体,符合下列条件的所有同分异构体有 种:
a.苯环上有3个取代基;
b.仅属于酯类,能发生银镜反应,且每摩该物质反应时最多能生成4 mol Ag。
其中苯环上的一氯代物有两种的结构简式 (任写出一种)。
(6)写出由Ⅰ到M的合成路线(用流程图表示):
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种金属A与B组成原电池时,A是正极。下列有关推断正确的是:
A.A的金属性强于B
B.电子不断由A电极经外电路流向B电极
C.A电极上发生的电极反应是还原反应
D.A的金属活动性一定排在氢前面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与化学概念有关的说法正确的是( )
A. 化合反应均为氧化还原反应
B. 金属氧化物均为碱性氧化物
C. 烧碱、纯碱、熟石灰都是碱
D. BaSO4、NaOH、HNO3都是强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
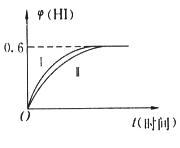
【题目】将1molI2(g)和2molH2(g)置于某2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) ![]() 2HI(g) △H<0,并在10min时达到平衡。HI的体积分数
2HI(g) △H<0,并在10min时达到平衡。HI的体积分数![]() (HI)随时间变化如图所示曲线(Ⅱ)。
(HI)随时间变化如图所示曲线(Ⅱ)。
(1)在此条件下,下列能说明该反应达到平衡状态的是___________(填序号)。
A.混合气体密度不再变化
B.反应混合物中H2的浓度不变
C.混合气体的颜色不再变化
D.每消耗1molH2同时消耗1molI2
(2)在达平衡过程中用HI(g)表示的反应速率为___________;I2(g)的平衡转化率为_______________。
(3)在此温度下,该反应的平衡常数K=_______(保留一位小数),若保持温度、体积不变,向已平衡的体系中再充入I2(g)和HI(g)各1mol,此时平衡___________(填“向左移动”“向右移动”或“不移动”)。
(4)若改变反应条件,在某条件下![]() (HI)的变化如曲线(Ⅰ)所示,则该条件可能是____________(填序号)。
(HI)的变化如曲线(Ⅰ)所示,则该条件可能是____________(填序号)。
①恒容条件下,降低温度
②恒温条件下,缩小反应容器体积
③恒温条件下,扩大反应容器体积
④恒温、恒容条件下,加入适当催化剂
(5)若保持温度不变,在另一相同的2L密闭容器中加入amolI2(g)、 bmolH2(g)和cmolHI(g)(a、b、c均大于0),发生反应达平衡时,HI体积分数仍为0.60,则a、b、c的关系为__________________(用一个含a、b、c的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知l.806×1023个X气体分子的质量为19.2g,则X气体的摩尔质量是
A. 16g B. 32 C. 64g/mol D. 32g/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com