
下列有关浓硫酸的叙述正确的是( )
①浓硫酸在常温下能够使铁、铝等金属钝化
②浓硫酸与铜加热反应后,铜片有剩余,硫酸完全反应
③浓硫酸具有吸水性,因而能使蔗糖炭化
④浓硫酸与铜加热反应后,铜片有剩余,向反应后的溶液中再加入铁片,会有氢气生成
⑤浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
⑥浓硫酸与铁加热反应后,铁片有剩余,生成的气体除水蒸气外为SO2
⑦浓硫酸具有强氧化性,常温下能与Cu发生剧烈反应
⑧浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2
A.①②③ B.①④
C.③⑤ D.⑥⑦⑧
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。对该电池的描述合理的是①溶液中硫酸的物质的量浓度保持不变;②Cu极上有气泡产生,发生还原反应;③Cu为负极,Zn为正极;④原电池在工作时电子由负极通过溶液流向正极;⑤该装置将化学能转变为电能( )
A.④⑤ B.③⑤ C.①② D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是巨大的化学资源库,下列有关海水综合利用说法正确的是( )
A.从海水中可以得到NaCl,电解熔融NaCl可制备金属Na
B.海水蒸发制海盐的过程中只发生了化学变化
C.海水的淡化,只需经过化学变化就可以得到
D.利用海水、铝、空气的航标灯的原理是将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )
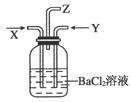
A.洗气瓶中产生的沉淀是碳酸钡 B.洗气瓶中产生的沉淀是硫酸钡
C.在Z导管出来的气体中无二氧化碳 D.洗气瓶中产生的沉淀是碳酸钡和硫酸钡
查看答案和解析>>
科目:高中化学 来源: 题型:
某氮肥厂氨氮废水中氮元素多以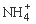 和NH3·H2O的形式存在,该废水的处理流程如下:
和NH3·H2O的形式存在,该废水的处理流程如下:
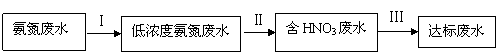

(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收。用离子方程式表示加NaOH溶液的作用
(2)过程Ⅱ:在微生物作用的条件下,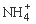 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:

第一步反应是 反应(选填“放热”或“吸热”),判断依据是
。1 mol 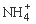 (aq)完全转化成
(aq)完全转化成  (aq)共与环境交换了 kJ热量。
(aq)共与环境交换了 kJ热量。
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是
查看答案和解析>>
科目:高中化学 来源: 题型:
在BaCl2溶液中通入SO2气体,溶液仍澄清;若将BaCl2溶液分盛到两支试管中,其中一支加入硝酸,另一支加入烧碱溶液,然后再通入SO2气体,结果两支试管都有白色沉淀生成。由此得出下列结论合理的是:①氯化钡有两性 ②两支试管中生成的白色沉淀均是亚硫酸钡 ③SO2有还原性和溶于水显酸性 ④升高pH使SO2水溶液中SO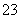 的浓度增大( )
的浓度增大( )
A.①② B.②③
C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列A~I九种物质之间的转化关系如图所示,其中部分生成物或反应条件已略去。已知A在常温下为黑色固体单质,常温下C、E、F都是无色气体。
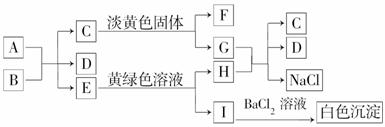
请回答下列问题:
(1)C的固体名称_______,F的化学式是________________________________。
(2)A与B反应的化学方程式是_______________________________________
________________________________________________________________________。
(3)G与H反应的离子方程式是____________________________________
________________________________________________________________________;
E转变为H和I的离子方程式是____________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

A.两者互为同分异构体,都是以Pt原子为中心的四面体结构
B.两者互为同分异构体,都是以Pt原子为中心的平面结构
C.两者为同一物质,都是以Pt原子为中心的四面体结构
D.两者为同一物质,都是以Pt原子为中心的平面结构
查看答案和解析>>
科目:高中化学 来源: 题型:
将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是( )
A.表面迅速变暗是因 为钠与空气中的氧气反应生成过氧化钠
为钠与空气中的氧气反应生成过氧化钠
B.“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液
C.最后变成碳酸钠粉末
D.该过程的所有化学反应均为氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com