
【题目】化学与生产、生活密切相关,下列说法正确的是
A.利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化过程
B.淀粉、油脂和蛋白质都是高分子化合物
C.煤经过气化和液化等物理变化可转化为清洁燃料
D.聚氯乙烯塑料薄膜可用作食品保鲜膜、一次性食品袋等
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 18g重水(D2O)所含的电子数为10NA
B. 常温常压下,0.3molNO2完全与水反应,转移的电子数为0.2NA
C. 标准状况下,22.4LCCl4中含有NA个CCl4分子
D. 常温下, 1L0.1mol/LCH3COONH4溶液中NH4+离子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国现阶段的能源结构仍以化石能源为主,为减少化石能源消耗、实现可持续发展,我国提出了“构建节约型社会”的口号。下列节约化石能源的措施不切实际的是
A. 充分利用太阳能 B. 充分利用风力和水力发电
C. 提高能源利用率 D. 不使用含碳的能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,下列说法正确的是
A. 厨房用品中食醋和纯碱都属于弱电解质 B. 淀粉是天然高分子,淀粉溶液属于胶体
C. 空气是由几种单质构成的混合物 D. 石油的分馏、煤的干馏都属于物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物0.1摩和标准状况下的氧气5.6升恰好反应完全,所得产物为CO2、CO、H2O(气),产物通过盛浓硫酸的洗气瓶,洗气瓶的质量增加了5.4克,再通过足量灼热的氧化铜,氧化铜的质量减轻了1.6克,再通过装有碱石灰的干燥管,干燥管增加了8.8克。
(1)求有机物的分子式,
(2)若此有机物能与钠反应,写出其结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过对煤的综合利用可得到洁净的燃料和多种化工原料,也可减少环境呢污染。煤的间接液化可得到甲醇。
(1)已知:CH3OH、H2的燃烧热(△H)分别为-726.5kJ/mol、-285.8kJ/mol,则常温下CO2和H2反应生成CH3OH和H2O的热化学方程式是____________。
(2)一定条件下,CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
①在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
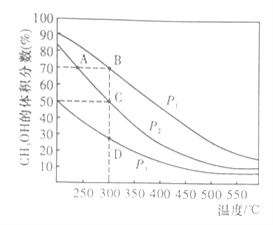
A、B、C三点平衡常数KA、KB、KC的大小关系是___________;压强:P1____P2(填“>”、“<”或“=”)
逆反应速率:v逆(A)______v逆(B)(填“>”、“<”或“=”)
在C点,CO的转化率为__________;
在C点,若再按物质的量之比1:2充入一定量的CO和H2,当其它条件不变,达到新的平衡时,CH3OH的体积分数__________(填“增大”、“减小”或“不变”)。
②若在恒温恒容条件下,能表示该可逆反应达到平衡状态的有__________。
A. 混合气体的密度保持不变
B. 混合气体的平均相对分子质量保持不变
C. 容器内的压强保持不变
D. 单位时间内每消耗1molCO的同时,生成2molH2
E. CO、H2、CH3OH的浓度保持不变
F. CO、H2、CH3OH的浓度之比为1:2:1
(3)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
H2CO3 | H2S | |
Ka1 | 4.4×10-7 | 1.3×10-7 |
Ka2 | 4.7×10-11 | 7.1×10-15 |
煤的气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为________;常温下,0.1mol·L-1NaHCO3溶液和0.1mol·L-1NaHS溶液的pH相比,pH较小的为______溶液(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:

(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为______.
(2)用电子式表示①与③形成化合物的过程______.:
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是______. ,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:______.
(4)①②③④四种元素的简单离子半径由大到小的顺序是______.(用离子符号和“>”表示)。
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是______.(用化学式和“>”表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生;
(2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是
A.K+一定存在 B.100 mL溶液中含0.01 mol CO32-
C.Cl-一定不存在 D.Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍具有优良的物理和化学特性,是高技术产业的重要原料。
(1)羰基法提纯镍涉及的反应为:Ni(s)+4CO(g)![]() Ni(CO)4(g)
Ni(CO)4(g)
①当温度升高时,![]() 减小,则△H________0(填“>”或“<”)。
减小,则△H________0(填“>”或“<”)。
②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是___________(填代号)
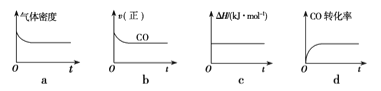
在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数 (填“增大”、“不变”或“减小”),反应进行3s后测得Ni(CO)4的物质的量为0.6mol,则0—3s内的平均反应速率v(CO)=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com