
【题目】下列物质的用途不正确的是( )
A.水玻璃可用作木材防火剂
B.用大量的二氧化硫作食品漂白剂
C.硅可用于制造太阳能电池
D.食醋可作食品酸味剂
科目:高中化学 来源: 题型:
【题目】为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如图: 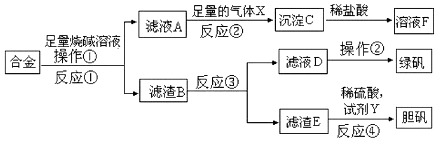
回答下列问题:
(1)操作①的名称为 , 沉淀C的化学式为 .
(2)在滤渣B中滴加稀硫酸时,发现反应速率比同浓度硫酸与纯铁粉反应要快,原因是 .
(3)在滤渣B中滴加的硫酸可用SO2制取,可按以下三步进行: 已知25℃、101kPa时:
2SO2(g)+O2(g)2SO3(g)△H1=﹣197KJ/mol
H2O(g)═H2O(l)△H2=﹣44KJ/mol
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=﹣545KJ/mol
则SO3(g)与H2O(l)反应的热化学方程式是 .
(4)设计实验方案,检测滤液D中含有的金属离子(试剂自选) .
(5)常温下,乙同学将绿矾配成约0.1molL﹣1FeSO4溶液,测得溶液的pH=3,请用离子方程式解释其原因 , 该溶液中c(SO42﹣)﹣c(Fe2+)=molL﹣1(填近似数值).
(6)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,则反应④的总反应化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
(1)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色,则该溶液呈性,原因是;(用离子方程式表示)
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于;
(3)已知在H2S溶液中存在下列平衡:H2S═HS﹣+H+①向H2S溶液中加入NaOH固体时,(不考虑温度变化)电离平衡向移动,(填“左”或“右”)c(H+) . (填“增大”、“减小”或“不变”)
②向H2S溶液中加入NaHS固体时,电离平衡向移动,(填“左”或“右”)c(S2﹣) . (填“增大”、“减小”或“不变”)
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是(填“A”或“B”);设盐酸中加入的Zn质量为m1 , 醋酸溶液中加入的Zn质量为m2 . 则m1m2 . (选填“<”、“=”、“>”) 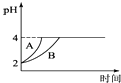
(5)难溶电解质在水溶液中存在溶解平衡.某MgSO4溶液里c(Mg2+)=0.002molL﹣1 , 如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于;(该温度下Mg(OH)2的Ksp=2×10﹣11)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com