
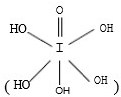
 和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:I
和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:I
| M |
| NA |
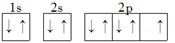 ,故答案为:p;
,故答案为:p;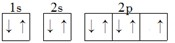 ;4s24p5;
;4s24p5;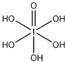 )中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4,故答案为:<;
)中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4,故答案为:<;| 7+1-2×2 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| M |
| NA |
| a3ρNA |
| 4 |
| a3ρNA |
| 4 |


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
 短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中正确的是( )
短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中正确的是( )| A、Y的最高价氧化物对应的水化物是强酸 |
| B、W的原子半径在同周期主族元素中最小 |
| C、W的非金属性比Z的弱 |
| D、Z的气态氢化物的稳定性在同主族元素中最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在熔融电解质中,O2-由负极移向正极 |
| B、通入丁烷的一极是正极,电极反应为:2C4H10+26e-+13O2-=4CO2+5H2O |
| C、通入空气的一极是负极,电极反应为:O2+4e-=2O2- |
| D、电池的总反应是:2C4H10+13O2→8CO2+10H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18gD2O中含有的电子数是10NA |
| B、1molBaCl2中含有的离子数是2NA |
| C、7.1gCl2与足量的NaOH溶液反应转移的电子数是0.2NA |
| D、1molCH4分子中共价键总数是4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com