
下列物质中属于电解质的是( )
①氢氧化钠②硫酸钡③铜④蔗糖⑤二氧化硫.
|
| A. | ①②⑤ | B. | ①② | C. | ③④ | D. | ①⑤ |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A. NaAlO2溶液中通入过量的CO2:2AlO2﹣+3H2O+CO2═2Al(OH)3↓+CO32﹣
B. 明矾溶液中滴加Ba(OH)2溶液至SO42﹣完全沉淀:Al3++Ba2++SO42﹣+3OH﹣═BaSO4↓+Al(OH)3↓
C. 200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br﹣+5Cl2═4Fe3++3Br2+10Cl﹣
D. 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO﹣+2Fe(OH)3═2FeO42﹣+3Cl﹣+H2O+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于价电子构型为3s23p4的粒子描述正确的是( )
|
| A. | 它的原子核外有三种形状不同的电子云 |
|
| B. | 它的原子核外电子共有16种不同的运动状态 |
|
| C. | 它可与H2反应生成的化合物为非极性分子 |
|
| D. | 核外电子轨道表示式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
|
| A. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
|
| B. | 氢氧化铜可溶于氨水说明氢氧化铜是两性氢氧化物 |
|
| C. | 在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3给出孤电子对 |
|
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤电子对,NH3提供空轨道 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)BCl3和NCl3中心原子的杂化方式分别为 和 .第一电离能介于B、N之间的第二周期元素有 种.
(2)若BCl3与XYm通过B原子与X原子间的配位健结合形成配合物,则该配合物中提供孤对电子的原子是 .
(3)BF3与一定量水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:
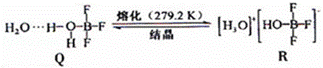
①晶体Q中各种微粒间的作用力不涉及 (填序号).
a.离子键 b.共价键 c.配位键 d.氢键e.范德华力
②R中阳离子的空间构型为 ,阴离子的中心原子轨道采用 杂化.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中两种物质在溶液中的反应可用同一离子方程式表示的是( )
|
| A. | Cu(OH)2+HCl;Cu(OH)2+CH3COOH | B. | NaHCO3+H2SO4;Na2CO3+HCl |
|
| C. | NaHCO3+NaOH;Ca(HCO3)2+NaOH | D. | BaCl2+H2SO4;Ba(OH)2+Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能大量共存,加入OH﹣有沉淀生成,加入H+有气体生成的一组离子是( )
|
| A. | K+、Mg2+、Cl﹣、HCO3﹣ | B. | K+、Cu2+、SO42﹣、Na+ |
|
| C. | NH4+、CO32﹣、NO3﹣、Na+ | D. | NH4+、Cl﹣、HCO3﹣、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向无水乙醇中加入浓H2SO4,加热至170℃,产生的气体通入酸性KMnO4溶液,紫红色褪去 | 使溶液褪色的气体是乙烯 |
| D | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
中学阶级介绍的电解原理的应用主要有三种:一是氯碱工业、二是电解精炼铜、三是电解冶金。下列关于这三个工业生产的描述中正确的是
A.电解精炼铜时,负极反应式:Cu2++2e-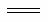 Cu
Cu
B.氯碱工业和电解精炼铜中,阳极都是氯离子放电放出氯气
C.在氯碱工业中,电解池中的阴极产生的是H2, NaOH在阳极附近产生
D.电解精炼铜时,应用粗铜作阳极、精铜作阴极,可溶性铜盐作电解质溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com