
 把一块镁铝合金投入到50mL1mol/L的HCl溶液里,待合金完全溶解后,往溶液里加入1mol/L的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示.下列说法中正确的是( )
把一块镁铝合金投入到50mL1mol/L的HCl溶液里,待合金完全溶解后,往溶液里加入1mol/L的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示.下列说法中正确的是( )| A. | 根据图象判断,镁铝合金与50mL1mol/L的HCl溶液恰好完全反应 | |
| B. | c值越大,合金中Mg的含量越高 | |
| C. | b值越大,合金中Al的含量越高 | |
| D. | 假设a=25,整个反应过程中,主要发生了6个离子反应 |
分析 根据图可知,首先发生的反应是中和过量的酸:H++OH-=H2O,然后是沉淀两种金属离子:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,最后是Al(OH)3的溶解:Al(OH)3+OH-=AlO2-+2H2O,由此分析解答.
解答 解:A、镁铝合金与50mL1mol/L的HCl反应,盐酸过量,故A错误;
B、c值越大,说明氢氧化铝消耗氢氧化钠的量越大,所以氢氧化铝的量越多,则合金中Al的含量越高,故B错误;
C、b值越大,合金中Al的含量越高,说明c-b的值越小,所以氢氧化铝的量越小,则合金中Al的含量越小,故C错误;
D、假设a=25,整个反应过程中,主要发生了镁铝与氢离子2个反应和0→a:H++OH-=H2O、a→b:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,最后是Al(OH)3的溶解:Al(OH)3+OH-=AlO2-+2H2O,共6个离子反应,故D正确;
故选:D.
点评 本题考查镁铝及其化合物的性质、结合图象计算,难度较大,清楚各阶段发生的反应是关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.89mol/L | B. | 0.82mol/L | C. | 0.78mol/L | D. | 0.60mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 购物尽量使用可反复使用的布袋 | B. | 保持饮水机24小时开启 | ||
| C. | 尽量避免使用一次性餐具 | D. | 随手关灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
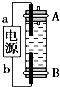 某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )| A. | 电源中a一定为负极,b一定为正极 | |
| B. | 可以用NaCl作为电解质,但不能用Na2SO4 | |
| C. | A、B两端都必须用铁作电极 | |
| D. | 阴极上发生的反应是:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲容器中的反应先达到化学平衡状态 | |
| B. | 两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量不相同 | |
| C. | 两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示 | |
| D. | 在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 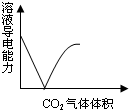 CO2通入澄清石灰水 | B. | 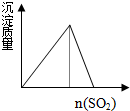 水玻璃中通入SO2 | ||
| C. | 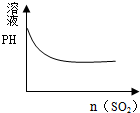 氯水中通入SO2 | D. |  NaOH溶液滴入Ba(HCO3)2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com