
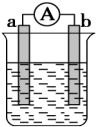
 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:分析 (1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,Al易失电子作负极、Cu正极,正极上氢离子得电子发生还原反应;
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置能自发进行氧化还原反应,能构成原电池,Al作负极、Mg作正极;
(3)燃料电池中,负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应.
解答 解:(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,Al易失电子作负极、Cu正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,
故答案为:2H++2e-=H2↑;
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置能自发进行氧化还原反应,能构成原电池,Al失电子作负极、Mg作正极,负极Al逐渐溶解,正极上生成氢气;
故答案为:能;a极铝片逐渐溶解,b极上有气泡产生;
(3)燃料电池中,负极上燃料失电子发生氧化反应,所以通入甲烷的电极为b,正极上氧化剂得电子发生还原反应,负极上甲烷失电子生成碳酸根离子和水,负极的反应为CH4+10OH--8e-=CO32-+7H2O,
故答案为:b;CH4+10OH--8e-=CO32-+7H2O.
点评 本题考查原电池原理,把握图中装置的分析及原电池的工作原理为解答的关键,侧重电解质溶液与电极的反应、转移电子的考查,题目难度中等,题目有利于培养学生对基础知识的应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 将过量SO2通入稀氨水中:SO2+NH3•H2O═HSO3-+NH4+ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 大理石溶于醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中NH3被还原 | B. | 该反应利用了Cl2的强氧化性 | ||
| C. | 若管道漏气遇氨就会产生白烟 | D. | 生成1mol N2有6mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18.0 L | B. | 27.0 L | C. | 31.4 L | D. | 33.6 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.1 g | B. | 25.4 g | C. | 33.2g | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向两种气体中加入适量水,振荡 | B. | 将两种气体分别通入AgNO3溶液中 | ||
| C. | 用湿润的淀粉KI试纸检验 | D. | 将两种气体分别通入FeCl2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 吸热反应发生过程中要不断从外界获得能量,放热反应不需要吸收外界能量 | |
| D. | 是放热反应还是吸热反应主要由反应物、生成物所具有的总能量的相对大小决定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com