
����Ŀ��ͨ�����ǰѲ�1 molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H)����ѧ��Ӧ����H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ�.
��ѧ�� | H��H | Cl��Cl | H��Cl |
����1 mol��ѧ��ʱ�ų������� | 436 kJ/mol | 243 kJ/mol | 431 kJ/mol |
�������Ȼ�ѧ����ʽ����ȷ���� (����)
A.1/2H2(g)��1/2Cl2(g)===HCl(g)��H����91.5 kJ/mol
B.H2(g)��Cl2(g)===2HCl(g)����H����183 kJ/mol
C.2HCl(g)===H2(g)��Cl2(g)����H����183 kJ/mol
D.1/2H2(g)��1/2Cl2(g)===HCl(g)��H����91.5 kJ/mol

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ��(CH2=CHCN)��һ����Ҫ�Ļ���ԭ�ϣ���ҵ�Ͽ�������ϩ������������������Ҫ�������б�ϩȩ(CH2=CHCHO)������(CH3CN)�ȣ��ش��������⣺
(1)����������ϩ���ԭ�ϱ�ϩ����һ����Σ���ԡ�ij�л�����������һ���ϩ����ͻȻ��ը����¼����������ĸ���ʹ������Ա���Կ�������֪��ϩ��ȼ����Ϊ2049 kJ/mol������ȼ�շ�Ӧ���Ȼ�ѧ����ʽΪ��____________________��
(2)ͼ��a��Ϊ��ϩ������뷴Ӧ�¶ȵĹ�ϵ���ߣ���߲��ʶ�Ӧ�¶�Ϊ460�档����460��ʱ����ϩ��IJ���________��������������������������Ӧ�¶��µ�ƽ����ʣ��ж�������_____________________������460��ʱ����ϩ����ʽ��͵Ŀ���ԭ����________��˫ѡ�����ţ�
A.�������Խ��� B.ƽ�ⳣ����� C.����Ӧ���� D.��Ӧ�������
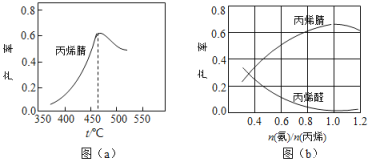
(3)��ϩ��ͱ�ϩȩ�IJ�����![]() �Ĺ�ϵ��ͼ��b����ʾ����ͼ��֪���
�Ĺ�ϵ��ͼ��b����ʾ����ͼ��֪���![]() ԼΪ________��������___________________��������������������ϩ�����������ԼΪ________��
ԼΪ________��������___________________��������������������ϩ�����������ԼΪ________��
(4)���Ա�ϩΪԭ�ϣ��ϳɻ�״��J���йع�������ͼ���¡���֪��ϩ�����ֽⷴӦ��ָ�ڴ��������£�ʵ��̼��̼˫�������Ż�λ�ķ�Ӧ����������ϩ���ӽ���ϩ����λ�����ɶ�ϩ����ϩ��
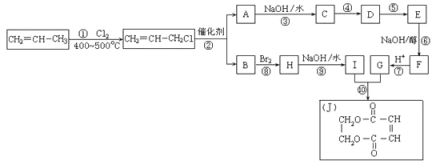
�ο���ѧ����ʽ��2CH2=CHCH3![]() CH3CH=CHCH3+CH2=CH2
CH3CH=CHCH3+CH2=CH2
i.�ٵķ�Ӧ������_____________������E�Ľṹ��ʽ��___________��
ii.�л�������C�ж���ͬ���칹�壬��д�����������������ܷ���������Ӧ������ͬ���칹��Ľṹ��ʽ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ�У�ʵ�ʲμӷ�Ӧ���������뻹ԭ�������ʵ���֮����ȷ����(����)
��KClO3��6HCl(Ũ)=KCl��3Cl2����3H2O��1��6
��3Cu��8HNO3(ϡ)=3Cu(NO3)2��2NO����4H2O��2��3
��SiO2��3C![]() SiC��2CO����1��2
SiC��2CO����1��2
��3NO2��H2O=2HNO3��NO��2��1
A.�٢�B.�ڢ�
C.�ڢ�D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹһþ���Ͻ��ĩ�ڹ���ϡH2SO4���ܽ⣬��������Һ�м���NaOH��Һ�����ɳ���������w�ͼ���NaOH��Һ�����V�Ĺ�ϵ��ͼ��ʾ����úϽ���þ����������֮��Ϊ�� ��
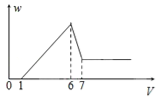
A. 2��3 B. 1��1 C. 4��3 D. 8��9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ҵ�ϼ��SO2�����Ƿ�ﵽ�ŷű��Ļ�ѧ��Ӧԭ����SO2+ H2O2+ BaCl2= BaSO4��+ 2HC1 ����NA��ʾ�����ӵ�������ֵ������˵������ȷ����
A. 0.1 molBaCl2��������������ԼΪ0.3 NA
B. 25��ʱ��pH=l��HC1��Һ�к���H+����ĿԼΪ0.1 NA
C. ��״���£�17gH2O2��������������ԼΪ9 NA
D. ����2.33gBaSO4����ʱ������SO2������ڱ�״����ԼΪ0.224L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܱ������������·�Ӧ��L(s)��aG(g) ![]() bR(g)���¶Ⱥ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ������ѹǿp1��p2���ɴ˿��ж�(����)
bR(g)���¶Ⱥ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ������ѹǿp1��p2���ɴ˿��ж�(����)
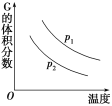
A.����ӦΪ���ȷ�Ӧ
B.G��ת�������¶����߶���С
C.��ѧ����ʽ�еļ�����a��b
D.����ѹǿ��������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaClO2��һ����Ҫ��ɱ����������Ҳ������Ư��֯��ȣ���һ������������ͼ��ʾ����ش��������⣺
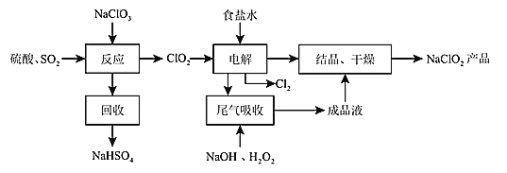
��1��NaClO2��ClԪ�صĻ��ϼ�Ϊ_____________��
��2��д������Ӧ������������ClO2�Ļ�ѧ����ʽ________________________��
��3����β�������������з����ķ�ӦΪ2NaOH + H2O2 + 2ClO2 = 2NaClO2 + O2�� + 2H2O �������������뻹ԭ�������ʵ���֮��Ϊ_________������3 mol ���ӷ���ת�ƣ�����__________L����״���£�O2���ɡ�
��4������Ч�Ⱥ���������������������������������������ָÿ�˺��������������������൱�ڶ��ٿ�Cl2��������������NaClO2����Ч�Ⱥ���Ϊ_____�����������λС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����KNO3������Ʒ�к���������KCl��BaCl2���ʣ�Ϊ���ᴿKNO3������õ�BaCl2����������ʵ�������

��1���������K2CO3��������Ӧ�����ӷ���ʽΪ_________________________________��
��2�������ͼ�����ʵ��ܽ�����߿�֪�����۵�������_________________��

��3��������Ϊ������֮ǰ��������������b��Ҳ�ܵõ������Ĺ���1������Ϊ�ù۵��Ƿ���ȷ������������______________________________________��
��4�����Ƶõ� KNO3�������� 200 mL0.2mol/L KNO3 ��Һ��
�ٱ�ʵ���õ�����������ƽ��ҩ�ס����������ձ�����ͷ�ιܡ���Ͳ������_______________��
�����������ʹ�����Ƶ�KNO3 ��Һ��Ũ��ƫ�ߵ���______________������ĸ����
A��û��ϴ���ձ��Ͳ����� B������ƿ�����������������ˮ
C������ʱ���ӿ̶��� D������ʱ���ӿ̶���
E�����ݺ�����ƿ������ҡ�ȣ����ú�Һ����ڿ̶��ߣ��ټ�ˮ���̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮϵ�����ӵ�ذ�ȫ���ܺá��۸�������Ի����Ѻã����ž���г�ǰ����ij�����ӵ�ع���ԭ����ͼ������ܷ�ӦΪ��2NaFePO4F + Na3Ti2(PO4)3![]() 2Na2FePO4F+ NaTi2(PO4)3
2Na2FePO4F+ NaTi2(PO4)3
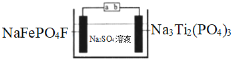
����˵���������
A.���ʱ��a�ӵ�Դ����
B.�ŵ�ʱ����Һ�е�Na+��NaFePO4F�缫�ϵõ��ӱ���ԭ
C.���ʱ�������ϵĵ缫��ӦΪNaTi2(PO4)3+2Na++2e��=Na3Ti2(PO4)3
D.�����ϣ��õ���ڳ���ŵ��������Һ�е�c(Na+)����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com