
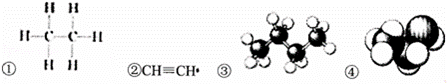
下列各项中,用来表示物质的组成或结构的模型是( )
|
| A. | ①②③④ | B. | ①和② | C. | ③和④ | D. | 只有① |
考点:
常见有机化合物的结构;结构式;结构简式;球棍模型与比例模型.
分析:
①是物质的结构式,只能确定其元素组成以及成键方式,不能确定其结构;
②是物质的结构简式,只能确定其元素组成以及成键方式,不能确定其结构;
③是丙烷的球棍模型,能正确表示出物质的组成与结构;
④是乙醇的比例模型,能正确表示出物质的组成与结构;据此选择即可.
解答:
解:①是乙烷的结构式,只能确定乙烷的元素组成以及成键方式,不能乙烷的结构,故错误;
②是乙炔的结构简式,只能确定乙炔元素组成以及成键方式,不能确定乙炔的结构,故错误;
③是丙烷的球棍模型,能正确表示出物质的组成与结构,故正确;
④是乙醇的比例模型,能正确表示出物质的组成与结构,故正确,故选C.
点评:
本题主要考查的是有机物的几种表示方法,结构简式与结构式不能确定其结构,球棍模型和比例模型可以确定结构,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
有三种物质AC2、B2C2、AD4,第二周期元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;元素D的负一价阴离子电子层结构与氩原子相同,则:
(1)A、B的元素名称分别为 、 .
(2)AD4分子其中含有的化学键类型为 键(选填“极性”或“非极性”).
(3)D的负一价阴离子的电子排布式为 ,B2C2的电子式为 ,属 (填“离子化合物”或“共价化合物”).
查看答案和解析>>
科目:高中化学 来源: 题型:
已知如下两个热化学反应方程式.
 (l)+H2(g)﹣→
(l)+H2(g)﹣→ (l)△H>0 ①
(l)△H>0 ①
 (l)+2H2(g)﹣→
(l)+2H2(g)﹣→ (l)△H<0 ②
(l)△H<0 ②
下列说法不正确的是( )
|
| A. | 反应①、②都属于加成反应 |
|
| B. | 在通常条件下,反应①、②都能自发进行 |
|
| C. | 反应①吸热、反应②放热的事实说明苯环中含有的并不是碳碳双键 |
|
| D. | 反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2﹣具有相同的电子层结构;离子半径:Z2﹣>W﹣;Y的内层电子总数是最外层电子数的5倍.下列说法中不正确的是( )
|
| A. | W、M的某种单质可作为水处理中的消毒剂 |
|
| B. | 电解YW2的熔融物可制得Y和W的单质 |
|
| C. | 相同条件下,W的氢化物水溶液酸性比Z弱 |
|
| D. | X、M两种元素形成的一种化合物与水反应可生成M的某种单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为:
2NaNH2+N2O═NaN3+NaOH+NH3;3NaNH2+NaNO3═NaN3+3NaOH+NH3↑.
回答下列问题:
(1)氮所在的周期中,电负性最大的元素是 ,第一电离能最小的元素是.
(2)基态氮原子的L层电子排布图为 .
(3)与N3﹣互为等电子体的分子为 (写出一种).依据价层电子对互斥理论,NO3﹣的空间构型为 .
(4)氨基化钠(NaNH2)和叠氮化钠(NaN3)的晶体类型为 .叠氮化钠的水溶液呈碱性,用离子方程式表示其原因: .
(5)N2O沸点(﹣88.49℃)比NH3沸点(﹣33.34℃)低,其主要原因是 .
(6)安全气囊的设计原理为6NaN3+Fe2O3 3Na2O+2Fe+9N2↑.
3Na2O+2Fe+9N2↑.
①氮分子中σ键和π键数目之比为 .
②铁晶体中存在的化学键类型为 .
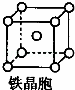
③铁晶体为体心立方堆积,其晶胞如图所示,晶胞边长为a cm,该铁晶体密度为 3 (用含a、NA的表达式表示,其中NA为阿伏加德罗常数).
查看答案和解析>>
科目:高中化学 来源: 题型:
.下列对有机物结构或性质的描述,错误的是( )
A. 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应
B. 苯酚钠溶液中通入CO2生成苯酚,则碳酸的酸性比苯酚弱
C. 等质量的乙烷和丙烯完成燃烧,丙烯生成的CO2多
D. 2,2﹣二甲基丙烷的一溴取代物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃A的相对分子质量为84.回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号) .
a.C7H12O2;b.C6H14;c.C6H14O;d.C7H14O3
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种.
①A的结构简式为 ;
②链烃A与Br2的CCl4溶液反应生成B,B与NaOH的醇溶液共热可得到D,D分子中无溴原子.请写出由B制备D的化学方程式: ;
③B与足量NaOH水溶液完全反应,生成有机物E,该反应的化学方程式: ;E与乙二醇的关系是 .
(3)若核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为3:2:1,则A的名称为 .
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=﹣Q1 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(l)△H=﹣Q2 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(g)△H=﹣Q3 kJ/mol
判断Q1、Q2、Q3三者关系正确的是()
A. Q1>Q2>Q3 B. Q1>Q3>Q2 C. Q3>Q2>Q1 D. Q2>Q1>Q3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com