
【题目】下列变化不属于化学变化的是( )
A.SO2使品红溶液褪色
B.氯水使有色布条褪色
C.活性炭使红墨水褪色
D.H2O2溶液使染料褪色
科目:高中化学 来源: 题型:
【题目】用铅蓄电池连接惰性电极电解一定量的CuSO4溶液,请回答下列问题:
(1)铅蓄电池放电时正极的电极反应式为________________________________;
(2)惰性电极电解CuSO4溶液的离子方程为_____________________;
(3)若电解一段时间后向电解池溶液中加入1molCu(OH)2·CuCO3,可以使该溶液恢复至原来的浓度和体积,则在该电解过程中转移电子的数目为___________,该电解过程中铅蓄电池中消耗的H2SO4和电解池中生成的H2SO4的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气排放的NO和CO都是有毒的气体,科学家正在研究利用催化技术将尾气中的NO和CO转变成无毒的CO2和N2,减少污染。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.0 kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221.0 kJ/mol
2C(s)+2O2(g)=2CO2(g) △H=-787.0 kJ/mol
则尾气转化反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H= 。
N2(g)+2CO2(g) △H= 。
(2)对于反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g),为了测定在某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如下表
N2(g)+2CO2(g),为了测定在某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/×10-4 mol/L | 3.00 | 2.25 | 1.75 | 1.36 | 1.00 | 1.00 |
c(CO)/×10-4 mol/L | 4.00 | 3.25 | 2.75 | 2.36 | 2.00 | 2.00 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前2s内的平均反应速率 υ(CO2)= mol/(Ls)。
②在该温度下,反应的平衡常数K= 。
(3)假设在恒容密闭容器中发生上述反应,下列有关说法正确的是 。
A.选用更有效的催化剂能提高尾气的转化率
B.升高反应体系的温度能提高反应速率, 提高尾气的转化率
C.相同温度下,若NO和CO的起始浓度分别为1.50×10-4 mol/L和2.00×10-4 mol/L,平衡时N2的体积分数比原平衡体系中N2的体积分数低
D.单位时间内消耗NO的物质的量等于生成CO2的物质的量时即达平衡状态

(4)用尾气NO2为原料可制新型硝化剂N2O5,原理:先将NO2转化为N2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有11.2 g KOH的稀溶液与1 L 0.1 mol/L的H2SO4溶液反应,放出11.46 kJ的热量,表示该反应中和热的化学方程式为( )
A.KOH(aq)+H2SO4(aq)===K2SO4(aq)+H2O(l) Δ H=-11.46 kJ/mol
B.2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-11.46 kJ/mol
C.2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ/mol
D.KOH(aq)+![]() H2SO4(aq)===K2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol
H2SO4(aq)===K2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种综合处理SO2废气的工艺流程。下列说法正确的是( )

A.向B溶液中滴加KSCN溶液,溶液变为血红色
B.溶液B转化为溶液C发生的变化的离子方程式为4H++2Fe2++O2===2Fe3++2H2O
C.溶液酸性A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+![]() O2(g)===H2O(g),反应过程中能量变化如下图,问:
O2(g)===H2O(g),反应过程中能量变化如下图,问:
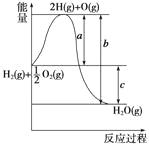
(1)a、b、c分别代表什么意义?
a______________;b____________;c__________。
(2)该反应是放热反应还是吸热反应?__________。ΔH大于零还是小于零?________
(3)若已知2H2(g)+O2(g)===2H2O(g) ΔH1=-Q1
2H2(g)+O2(g)===2H2O(l) ΔH2=-Q2
则ΔH1______ΔH2,Q1______Q2(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在101 kPa时,足量H2在1 mol O2中完全燃烧生成2 mol液态水,放出571.6 kJ的热量,H2的燃烧热为______,表示H2燃烧热的热化学方程式为___________________ 。
(2)1.00 L 1.00 mol·L-1硫酸与2.00 L 1.00 mol·L-1 NaOH溶液完全反应,放出114.6 kJ的热量,该反应的中和热为________,表示其中和热的热化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应速率、化学平衡的说法中错误的是( )
A.其它条件不变时,升高温度化学反应速率加快
B.其它条件不变时,增大浓度化学反应速率加快
C.当反应物的浓度与生成物的浓度相等时,化学反应达到化学平衡
D.当正反应的速率与逆反应的速率相等时,化学反应达到化学平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com