
【题目】Ⅰ.按如图所示装置进行实验,并回答下列问题:
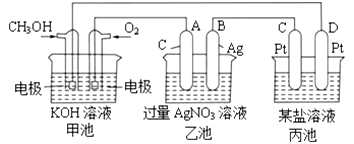
(1)甲池,通入CH3OH(甲醇)的电极反应式为______________________。
(2)乙池中的总反应化学方程式为______________________。
(3)当甲池中消耗O20.56L(标准状况下)时,理论上乙池中B极的质量增加__________g;此时丙装置中___________(填“c”或“d”)电极折出1.20g金属,则按丙装置中的的某盐溶液可能是__________________(填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
Ⅱ.SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控利和治理是优化我们生存环境的有效途径。
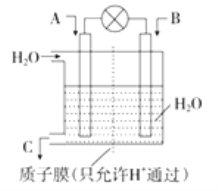
(4)利用化学原理将C0、SO2转化为重要化工原料,装置如图所示:
①若A为CO,B为H2,C为CH3OH,则通入CO一极为____________________极。
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为____________________。
③若A为NO2,B为O2,C为HNO3,则正极的电极反应式为____________________。
【答案】CH3OH—6e-+ 8OH-=CO32-+6H2O 4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3 10.8 d bd 正 SO2+2H2O-2e-=SO42-+4H+ O2+4e-+4H+=2H2O
4Ag+O2↑+4HNO3 10.8 d bd 正 SO2+2H2O-2e-=SO42-+4H+ O2+4e-+4H+=2H2O
【解析】
(1)甲池为原电池,燃料在负极失电子发生氧化还原反应在碱溶液中生成碳酸盐,甲池中通入CH3OH电极的电极反应为:CH3OH-6e-+8OH-═CO32-+6H2O,故答案为:CH3OH-6e-+8OH-═CO32-+6H2O;
(2)乙池是电解池,A为阳极,B为阴极,电池中是电解硝酸银溶液生成银,硝酸和氧气,电池反应为:4AgNO3+2H2O ![]() 4Ag+O2↑+4HNO3,故答案为:4AgNO3+2H2O
4Ag+O2↑+4HNO3,故答案为:4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3;
4Ag+O2↑+4HNO3;
(3)当甲池中消耗O20.56L(标准状况下)时,转移电子为0.56L /22.4L/mol×4=0.1mol,乙池中A电极上氢氧根离子放电、阴极上银离子放电,B(Ag)极的质量增加0.1mol×108g/mol=10.8g;丙池是电解池,阴极上金属离子放电析出金属单质,则金属元素在氢元素之后,丙池d电极析出1.20g金属,说明丙池中电解质是含有氧化性较强的金属阳离子在阴极得电子析出金属,不可能是镁离子和钠离子的盐溶液,则AC错误,此时转移电子为0.,1 mol,若是二价金属,金属的摩尔质量是24g/mol,无对应金属单质,若是一价金属,金属的摩尔质量是120g/mol,无对应金属单质,则只可能为铜银混合物,故选bd,故答案为:bd;
(4) ①燃料电池中,通入氧化剂的电极是正极、通入还原剂的电极是负极,该反应中C元素化合价由+2价变为-2价、H元素化合价由0价变为+1价,所以CO是氧化剂,则通入CO的电极为正极,故答案为:正;
②若A为SO2,B为O2,C为H2SO4,负极上二氧化硫失电子和水反应生成硫酸根离子和氢离子,电极反应式为SO2+2H2O-2e-=SO42-+4H+,故答案为:SO2+2H2O-2e-=SO42-+4H+;
③若A为NH3,B为O2,C为HNO3,则正极发生还原反应,氧气得电子生成水,电极方程式为O2+4e-+4H+═2H2O,故答案为:O2+4e-+4H+═2H2O。


科目:高中化学 来源: 题型:
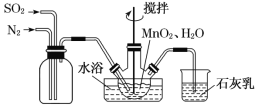
【题目】MnSO4是制备高纯MnCO3的中间原料。实验室用如图所示装置可制备少量MnSO4溶液,反应原理为MnO2+H2SO3=MnSO4+H2O。下列说法错误的是( )
A. 若实验中将N2换成空气,则反应液中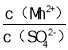 的浓度之比变大
的浓度之比变大
B. 缓慢通入混合气体可提高SO2的转化率
C. 若不通N2,则烧瓶中的进气管口容易被堵塞
D. 石灰乳对尾气的吸收效果比澄清石灰水更好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与我们的生产生活联系紧密,下列有关说法不正确的是( )
A. 人工固氮过程和乙酸乙酯的制备反应均为有限度的
B. 用漂白粉进行泳池消毒和用铁罐保存冷的浓硫酸都利用了化学物质的强氧化性
C. 高炉炼铁和用粮食酿酒的化学反应中都有二氧化碳生成
D. 豆浆的丁达尔效应和肥皂的去污过程发生的均为化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列化学方程式,并标明反应类型.
(1)CH4+Cl2![]() _____,_____;(只写产物均为气体的一个)
_____,_____;(只写产物均为气体的一个)
(2)CH2=CH2+Br2→__________,____________;
(3)![]() +Br2
+Br2![]() _________,_____。
_________,_____。
(4)与乙烯和氢气的加成产物互为同系物的是_____(填写编号)。
a C2H2 b C6H6 c C5H12 d C2H6O
(5)请写出乙烯加聚反应方程式_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)等质量的![]() 和
和![]() ,物质的量之比为______,在相同条件下的体积之比为_______,原子数之比为________.
,物质的量之比为______,在相同条件下的体积之比为_______,原子数之比为________.
(2)同温同压下,相同体积的![]() 和
和![]() 的质量比为_________。
的质量比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组粒子在溶液中可以大量共存,且加入或通入试剂X后,发生反应的离子方程式也正确的是
选项 | 微粒组 | 加入试剂 | 发生反应的离子方程式 |
A |
| 过量HC1 |
|
B |
| 过量 |
|
C |
| 过量 |
|
D | I-、Cl-、H+、SO42- | 过量 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示A处通入潮湿的Cl2,关闭活塞B时D中干燥的红色布条颜色无变化;打开活塞B时D处干燥的红色布条褪色,则C中的试剂(足量)不可能是
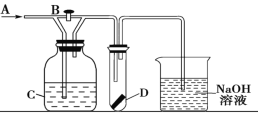
A.饱和氯化钠溶液B.氢氧化钙悬浊液C.饱和碳酸钠溶液D.浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目提供的溶度积数据进行计算并回答下列问题:
(1)T℃时,在Ca(NO3)2溶液中加入(NH4)2CO3溶液后过滤,若测得滤液中c(![]() )=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。
)=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。
[已知c(Ca2+)≤10-5 mol·L-1时可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
(2)已知25℃时,Ksp[Mg(OH)2]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为________。
(3)向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10-10,忽略溶液混合后体积的变化,请计算:
①完全沉淀后,溶液中c(Ag+)=__________________________。
②完全沉淀后,溶液的pH=________。
③如果向完全沉淀后的溶液中继续加入50 mL 0.001 mol·L-1的盐酸,是否有白色沉淀生成?________(填“是”或“否”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com