
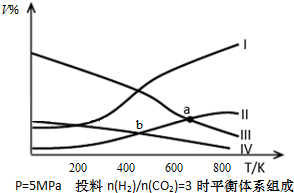
| A、表示CH3CH2OH组分的曲线是Ⅳ |
| B、图中曲线交点a对应的CO2转化率为40% |
| C、图中曲线交点a、b对应的上述反应平衡常数:Ka>Kb |
| D、若甲乙两个密闭容器起始是的容积,温度及投料方式均相同,甲:恒温恒压,乙:恒温恒容,反应达平衡时CH3CH2OH产率:甲<乙 |
| 2 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |


科目:高中化学 来源: 题型:
| A、除去CO2气体中的HCl:通过足量的饱和碳酸钠溶液 |
| B、除去粗盐中少量的MgCl2:溶解后,加入过量的NaOH溶液,过滤后加适量的盐酸,蒸干 |
| C、除去FeCl2溶液中的FeCl3:加入足量的铜粉,过滤 |
| D、除去Al2O3中的少量SiO2:加入足量的NaOH溶液,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.6 g Na完全转化成Na2O和Na2O2的混合物,生成物中阴离子总数为0.1 NA |
| B、标准状况下,11.2L Cl2与足量的铁反应转移的电子数为NA |
| C、将100mL 0.1mol?L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA |
| D、物质的量浓度为0.5 mol/L的NaCl溶液中,含有Cl-个数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
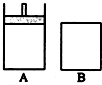 A容器是能 保持恒压的密闭容器,有一个能移动的活塞.B容器是保持恒容的密闭容器(如图所示),开始时,向A和B容器中分别充入2mol SO2 与1mol O2的混合气体,并且使A与B的容积相等,在一定温度下反应:2SO2(g)+O2(g)?2SO3(g)+Q(Q>0).
A容器是能 保持恒压的密闭容器,有一个能移动的活塞.B容器是保持恒容的密闭容器(如图所示),开始时,向A和B容器中分别充入2mol SO2 与1mol O2的混合气体,并且使A与B的容积相等,在一定温度下反应:2SO2(g)+O2(g)?2SO3(g)+Q(Q>0).查看答案和解析>>
科目:高中化学 来源: 题型:

| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、MgCl2(熔融)
| ||||
B、Al2O3+3C
| ||||
C、Fe2O3+3CO
| ||||
D、2Ag2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com