
分析 (1)根据量热计的构造和实验步骤来确定实验的仪器;中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是:保温、隔热、减少实验过程中的热量散失;
(2)为了保证HCl完全反应,碱应过量;温度过低,散热加快,对实验结过造成的误差较大;
(3)先根据Q=m•c•△T计算反应放出的热量,然后根据△H=-$\frac{Q}{n}$kJ/mol计算出反应热;
(4)根据实验的关键是保温,如果装置能量散失,则会导致结果偏低,如果装置得到能量,则会导致结果偏高,
A.根据不盖硬纸板,会有一部分热量散失;
B.根据金属的导热性很好,会导致热量的散失;
C.根据相同浓度和体积的硝酸代替稀盐酸都是稀的强酸,对实验无影响;
D.NaOH固体溶于水放热,温度升高.
解答 解:(1)中和热测定的实验中,用到的玻璃仪器有大烧杯、小烧杯、温度计、量筒、环形玻璃搅拌棒;大小烧杯之间填满碎泡沫塑料的作用是:保温、隔热、减少实验过程中的热量散失,
故答案为:量筒;环形玻璃搅拌棒;隔热、减少实验过程中热量的损失;
(2)NaOH的浓度大于HCl的浓度,使盐酸完全被中和,减少了盐酸挥发对实验的影响;如果温度过低,散热加快,对实验结过造成的误差较大,
故答案为:保证盐酸完全被中和;散热太快;
(3)0.50mol•L-1HCl和0.55mol•L-1的NaOH溶液各50mL进行中和反应,生成水的物质的量为:0.05L×0.50mol•L-1=0.025mol,溶液的质量为:100ml×1g/ml=100g,设反应前后的温度值分别用t1和t2表示,温度变化的值△T=t2-t1,则生成0.025mol水放出的热量为Q=m•c•△T=100g×4.18J/(g•℃)×(t2-t1)=100×4.18×(t2-t1)×10-3kJ;
所以实验测得的中和热为:△H=-$\frac{100×4.18({t}_{2}-{t}_{1})×1{0}^{-3}}{0.025}$kJ/mol,
故答案为:100×4.18×(t2-t1)×10-3;-$\frac{100×4.18({t}_{2}-{t}_{1})×1{0}^{-3}}{0.025}$;
(4)A.不盖硬纸板,会有一部分热量散失,使测得的△H数值偏小,故A错误;
B.用环形铜丝搅拌棒代替环形玻璃搅拌棒,金属的导热性很好,会导致热量的散失,使测得的△H数值偏小,故B错误;
C.相同浓度和体积的硝酸代替稀盐酸都是稀的强酸,对实验无影响,使测得的△H数值不变,故C错误;
D.NaOH固体溶于水放热,温度升高,使测得的△H数值偏大,故D正确;
故答案为:D.
点评 本题考查热反应热的测定与计算,题目难度大,注意理解中和热的概念以及测定反应热的原理,明确常见化学实验的基本操作方法,试题培养了学生的分析能力及化学实验能力.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:解答题
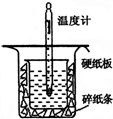 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用广泛pH试纸测得饱和氯水的pH约为2.2 | |
| B. | 用量筒量取7.60 mL 0.1 mol•L-1盐酸 | |
| C. | 用图1所示的操作可检查装置的气密性 | |
| D. | 实验室用图2所示的装置制取少量的NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
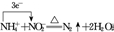 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解 加适量BaCl2溶液 过滤 | |
| B. | 溶解 加适量CaCl2溶液 过滤 | |
| C. | 溶解 加适量Ca(OH)2溶液 过滤 | |
| D. | 溶解 加适量盐酸 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和②产物的阴阳离子个数比不相等 | |
| B. | ①和②生成等物质的量的产物时,转移电子数不同 | |
| C. | 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | |
| D. | 反应:Na2O2(s)+2 Na(s)=2Na2O(s)△H=-317kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠着火用泡沫火器扑灭 | |
| B. | 苯酚沾在手上,应马上用NaOH溶液洗 | |
| C. | 皮肤上沾有浓硫酸,立即用量水冲洗 | |
| D. | 酒精灯在桌上歪倒失火后,立即用湿布盖上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com