
(11分)

根据信息回答下列问题:
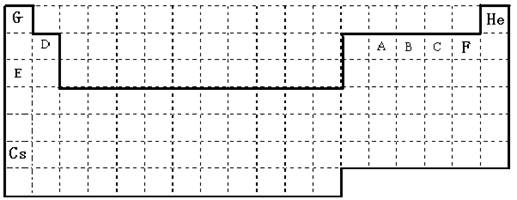
(1) 上表中实线是元素周期表的部分边界,请你用实线标出表的上边界,并把符合下列要求的元素的元素符号标在表中对应位置处。
① 最高价氧化物的水化物碱性最强(放射性元素除外)。
② 电负性最大。
③ 第一电离能对大。
(2)F元素的原子核外有25个运动状态不同的电子,F元素是 (名称),F2+的未成对电子数是_____ ,与F之具有相同最高正价的另一同周期元素的单质在常温下的状态为 。(填固态、液态、气态)
(3)列举一种由A、C、E、G四种元素组成的盐 。
(4)D的最高价氧化物对应的水化物属两性化合物,证明这一结论的有关离子方程式为_______________________________、_____________________________
(5)元素M基态原子中次外层有5个未成对电子而最外层只有一个电子; MCl3能与B和C的氢化物共同形成配位数为6的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。MCl3形成的配合物的化学式为_____ ___(用具体元素符号表示)。
(1)
(2)锰 5 液态 (3)NaHCO3等有机羧酸的钠盐均可(合理答案均军给分)
(4)Be(OH)2+2H+===Be2++2H2O Be(OH)2+2OH-===BeO+2H2O
(5)[Cr(NH3)4(H2O)2]Cl3
【解析】(1)考查元素周期表的结构。最高价氧化物的水化物碱性最强Cs,电负性最大是F,第一电离能最大的稀有气体He。
(2)F元素的原子核外有25个运动状态不同的电子,所以F元素是锰元素。根据构造原理可知,F2+的未成对电子数是5. 与锰具有相同最高正价的另一同周期元素是溴元素,其单质在常温下是液态。
(3)A、C、E、G四种元素分别是C、O、Na、H,所以该盐可以是碳酸氢钠或醋酸钠等。
(4)氢氧化物具有两性,则既能和酸反应生成盐和水,也能和碱反应生成盐和水。
(5)元素M基态原子中次外层有5个未成对电子而最外层只有一个电子,则M是铬元素。氨气和水的物质的量之比为2∶1,三个氯离子位于外界,所以结构简式为[Cr(NH3)4(H2O)2]Cl3。


科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质或结构信息 | 单质常温下为固体,难溶于水易于溶CS2.能形成2种二元含氧酸. | 原子的M层有1个未成对的p电子.核外p电子总数大于7. | 单质曾被称为“银色的金子”.与锂形成的合金常用于航天飞行器.单质能溶强酸和强碱. | 原子核外电子层上s电子总数比p电子总数少2个.单质和氧化物均为空间网状晶体,具有很高的熔、沸点. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质或 结构 信息 |
室温下单质呈粉末状固体,加热易熔化;单质在氧气中燃烧,发出明亮的蓝紫色火焰 | 单质常温、常压下是气体,能溶于水;原子的M层上有7个电子 | 单质质软、银白色固体、导电性强;单质在空气中燃烧发出黄色的火焰 | 原子最外电子层有4个电子;单质为空间网状晶体,具有很高的熔、沸点 |


查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质 结构 信息 |
室温下单质是粉末状固体,加热易熔化. 单质在空气中燃烧生成的气体是形成酸雨的主要污染物之一. |
单质常温、常压下是黄绿色气体,能溶于水. | 单质质软、银白色固体、导电性强. 单质在空气中燃烧发出黄色的火焰. |
原子最外层电子层上s电子数等于p电子数. 单质是一种常见的半导体材料. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素符号 | 元素性质或结构信息 |
| A | 原子核外L层未成对电子数最多 |
| B | 原子半径是短周期主族元素中最大的 |
| C | 地壳中含量最多的金属元素 |
| D | 原子核外有五种不同能量的电子,且最外层有2对成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | |
| 原子结构 | 失去电子后变成质子, | 最外层电子数是次外层电子数的3倍. | L层电子数等于K层和M层电子数之和. | 最外层电子排布为(n+1)sn(n+1)p(n+3). | |
| 物质性质 | 其最高价氧化物对应水化物的碱性是短周期元素中最强的. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com